 Udruženje vetrinara praktičara Srbije - UVPS
Udruženje vetrinara praktičara Srbije - UVPS
Tkivne protozoarne bolesti goveda
Autor:
Dr sci. vet. med. Ivan Pavlović - Naučni institut za veterinarstvo Srbije
Kratak sadržaj: Protozoarne infekcije su stalni pratilac farmskog držanja goveda. Nastanak i tok ovih oboljenja, uslovljen je prisustvom uzročnika, prijemčivih domaćina, ambijenta u objektima i životne sredine. U intezivnom uzgoju, svi navedeni elementi su potencirani, često u negativnom smislu s obzirom da takav odgoj ima i prednosti i mana. U ovakvom odgoju se nalaze velike aglomeracije u ograničenom prostoru, a opasnost od nastanka i širenja bolesti se povećava uporedo s gustinom aglomeracije. Što je veći broj životinja na manjem prostoru, mogućnost širenja infekcija je veća zbog toga što su uslovi smeštaja i ishrane u određenom vremenu istovetni i podjednako se povoljno ili negativno odražavaju na sve jedinke. Bez obzira na činjenicu da nanose velike gubitke govedarskoj proizvodnji, a uz to su neke i zoonotskog karaktera, infekcijama koje izazivaju protozoe se pridaje mnogo manji značaj nego helmintozama. Cilj ovog rada je upoznavanje sa najznačajnijim protozoarnim infekcijama goveda.
Ključne reči: bolesti, goveda, protozoe
Uvod
Protozoarne infekcije se najčešće pojavljuju kod mladih životinja (Geurden i sar., 2005, Ballweber, 2009, Marskole i sar., 2016, Campigotto i sar., 2017). Zbog nespecifičnih simptoma koji umnogome podsećaju na oboljenja bakterijske ili virusne etiologije, često se ne dijagnostikuju i zanemaruju, a mnogo manje su izučavane u našoj zemlji. U Srbiji, osim za pojedine bolesti kao što su kriptosporidioza i neosporoza, za ostale protozoarne infekcije postoje samo šturi podaci, ponekada stari i po pedesetak godina. Istraživanja novijeg datuma su tek otpočela tako da se ne može sa preciznošću znati ni prevalenca ni incidenca ovih infekcija, niti u farmskom niti u individualnom uzgoju goveda (Pavlović i Rogožarski, 2017). Da bi se, makar delimično, upotpunilo saznanje o ovim parazitozama, ovde je dat prikaz najznačajnih protozoarnih infekcija koje su zabeležene u Srbiji. Pri tome nisu obuhvaćene krvne protozoe koje zahtevaju poseban prikaz, kao ni njihovi vektori.
Kokcidioza
Kada se kaže kokcidioza, uobičajeno se misli na oboljenje koje uzrokuju protozoe iz familije Eimeridae. Kokcidije su intracelularni paraziti, strogo specifični za vrstu domaćina i za segment digestivnog trakta u kome parazitiraju. Životni ciklus kokcidija je direktan i vrlo kratak (manje od 7 dana). Oociste izbačene fecesom sporulišu u spoljašnjoj sredini za 1 do 2 dana. Ovo se naziva faza sporogonija i tokom nje se stvaraju sporociste čiji broj je karakterističan za svaki rod. Kada prijemčive jedinke unesu infektivne oociste, u digestivnom traktu se oslobađaju sporozoiti i počinje prvo bespolni, a potom polni ciklus parazita koji rezultira izlučivanjem oocisti fecesom. Infekcija nastaje hranom i vodom kontaminiranom oocistama (Pavlović i Rogožarski, 2017).
Kokcidioza goveda je akutno ili hronično oboljenje koje je u pojedinim zemljama, po svom značaju, u vrhu parazitskih obolenja (Nemačka, Holandija, Danska, UK, Iran). Javlja se uglavnom kod mlađih kategorija, a kod starijih životinja ukoliko je provocirana uslovima koji dovode do slabljenja imuniteta (stres, transport, neka od gastrointestinalnih oboljenja druge etiologije ili mikotoksini u hrani).
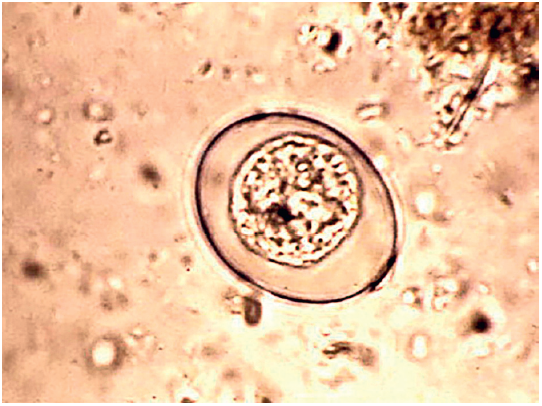
Slika 1. E. bovis
Najpatogenije vrste su E. bovis i E. zurni, a patogeno dejstvo ispoljavaju i E. alabamensis i E. auburensis (Teankum i sar., 2003).
Mesto parazitiranja su tanka creva. Prvi simptomi se pojavljuju 2–3 dana po infekciji, u vidu dugotrajnog upornog proliva neprijatnog mirisa, sa primesama krvi i sluzi. Dolazi do gubitka apetita, opšte slabosti i brzog mršavljenja, a ako bolest duže traje, nastaje anemija (Fitzgerald,1967). Crevna peristaltika je ubrzana sa stalnim tenezmima koji mogu uzrokovati i prolapsus rektuma. Kod teladi i mlađih životinja, tok bolesti je najčešće akutan i teži, dok se kod starijih životinja sa stečenim imunitetom javlja u blažem obliku (Fitzgerald, 1975). Kod starijih životinja je klinički manifestna kokcidioza, posledica slabljenja imuniteta izazvanog nekim drugim uzrokom (Ahmed i Soad, 2007).
Lokalizacija patoloških promena zavisi od vrste Eimeria. Tako E. zuernii oštećuje epitel sluznice cekuma, kolona i rektuma, a E. bovis sluznicu tankog creva kao i E. alabamensis i E. auburnensis (Heidari i sar., 2014). Kod mešovitih infekcija, zahvaćene su sve partije creva. Oštećenje crevnog epitela je direktna posledica intenzivnog razmnožavanja kokcidija i nastaju polja sa uništenim epitelom, pokrivena sa sluzi i fibrinom (Taylor, 2000). Kod težih infekcija, nastaju i nekroze sluznice u vidu ulcera. Sadržaj creva je sa primesama krvi, a u zadnjim partijama i sa krvnim ugrušcima. On se sastoji od deskvamisanog epitela, fibrina, eritrocita i velikog broja razvojnih oblika i oocisti kokcidija. Zavisno od dužine i jačine infekcije, nastaje kataralni ili hemoragični enteritis. Leševi uginulih životinja su kahektični, zaprljanog zadnjeg dela tela i repa, a posle duge bolesti se sreće i prolapsus rektuma (Thomas, 1994, Yatoo, 2013).
Dijagnoza se postavlja nalazom oocisti u izmetu, odnosno koprološkim pregledom. Terapija se vrši sulfametazinom u dozi od 100 mg/kg tokom 4 dana, sulfakvinoksalinom 15 mg/kg i amprolijumom 10 mg/kg tokom 5 dana. U preventivi se koriste jonoformni antibiotici: monenzin 1 mg/kg tokom mesec dana ili lasalocid 0,5–1 mg/kg p/o u hrani (Pavlović i Rogožarski, 2017).
Kriptosporidioza
Kriptosporidioza je dugo smatrana komisualnim oboljenjem, a kasnije je ustanovljeno da se radi o opasnim patogenima zoonotskog karaktera (Hunter i Thompson, 2005). Kriptospore ispoljavaju monoksenost prema klasi kičmenjaka u kojoj se nalazi domaćin, tako da je interspecijska infekcija moguća samo u tom obimu (Sevinc, 2004). Za razliku od drugih kokcidija, koje se u toku šizogonične faze implantiraju u mikroviluse creva, kriptospore formiraju parazitofornu vakuolu u mikrovilusu i ona se nalazi između spoljašnje membrane i citoplazme mikrovila. Prskanjem ovih vakuola nastaju mnogo ozbiljnije lezije i oštećenja crevnog epitela nego pri infekcijama drugim vrstama kokcidija (Taylor i Webster, 1998). Seksualni deo (gametogonija) je identičan kao kod drugih kokcidija, a tek oplođene oociste pre ekskrecije nastavljaju razvoj intracitoplazmatično i kao infektivne oociste napuštaju domaćina. Kriptosporidioza je česta parazitska infekcija od koje klinički oboljeva telad do 10 dana starosti (Xiao i Herd,1994).
Uzročnici oboljenja goveda su najčešće Cryptosporidium parvum i C. bovis. Način prenošenja je peroralna infekcija oocistama putem kontaminirane hrane i vode (Soltane i sar., 2007). Mesto parazitiranja je mikrovilusni epitel tankih creva i kolona (Ayinmode i Fagbemi, 2010, Adamu i sar., 2015). Klinička slika je uočljiva samo kod mlađih životinja u vidu dijareje, gubitka apetita i iznurenosti, a moguća su i uginuća. (Feitosa i sar., 2008).
Najčešći patoanatomski nalaz je edem i oštećenje mikrovilusnog sloja sluznica tankog creva sa mukofibrinoznim slojem (Olson i sar., 2004).
Slika 2. Cryptosporidium sp.
Dijagnoza se kod svih životinja vrši nalazom oocisti u izmetu (razmaz izmeta bojen po Zeihl-Nilsenu, flotacija). Terapija još nije u potpunosti rešena, mada su povoljni efekti postignuti primenom sulfapreparata (Pavlović i Rogožarski, 2017).
Giardiaza
Giardia duodenalis je flagelata koju smatraju najčešćom kod ljudi i životinja. Infekcija se prenosi cistama (otpornim oblicima uzročnika) koji se nalaze u izmetu životinja i čoveka a infekcija nastaje zagađenom vodom ili hranom (Hunter i Thompson, 2005). Giardia duodenalis (syn. G. intestinalia, G. lamblia) se javlja u vidu ciste jajastog oblika i vegetativnog oblika koji je je kruškolikog izgleda sa 8 bičića.
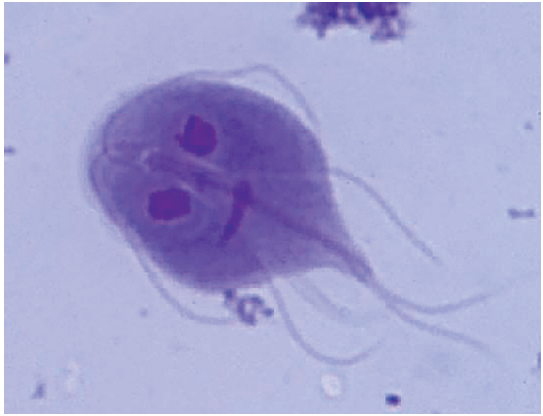
Slika 3. Giardia duodenalis
Mesta parazitiranja su sluzokoža tankog creva, žučne kesice i želuca. Nakon ulaska cisti u digestivni trakt, oslobađaju se vegetativni oblici Giardia koji će se zadržavati na površini crevnih resica, razmnožiti se i posle određenog vremena, encistirati (postati otporni na nepovoljne uslove okoline). Samo tako encistirana Giardia sposobna je da preživi i zarazi druge životinje (Olson i sar., 2004).
Bolest nastaje uglavnom kod životinja sa oslabljenim imunitetom, mladih životinja (teladi) i onih jedinki koje su u sebe unele veoma veliki broj cisti. Glavni klinički znak je proliv koji može da bude akutan ili hroničan, a može da se pojavljuje povremeno ili da traje stalno (Xiao i Herd, 1994). Proliv je tipičnog svetlog izgleda i neugodnog mirisa (zbog velike količine nesvarene masti). Zbog učestalog proliva, životinje slabo jedu ili nemaju apetit i mršave (Szostakowska i sar., 2004). Patoanatomski nalaz je vezan za promene u zidu creva koji je hemoragičan i sličan kao kod drugih obolenja izazvanih protozoama. Često je infekcija Giardijom praćena nekom virusnom, bakterijskom ili parazitarnom infekcijom što otežava i dijagnostiku i terapiju.
Dijagnoza se postavlja na osnovu kliničke slike i nalazom parazita u izmetu. Terapija se sprovodi metronidazolom, tinidazolom ili ornidazolom kao i orvažilom i albendazolom (Pavlović i Rogožarski, 2017).
Toksoplazmoza
Toksoplazmoza je jedna od najrasprostranjenijih parazitskih zoonoza. Prema procenama WHO, na osnovu seroloških pregleda, više od 700 miliona ljudi u svetu je inficirano sa T. gondii. Toxoplasma gondii je cistotvorna kokcidija koja za prvog domaćina ima mačke, a prelazni domaćini su sisari, gmizavci i ptice (više od 280 vrsta, ukljućujući i čoveka) (Alford i sar.,1975). Peroralna infekcija pravog domaćina (mačke i drugih felida) dovodi do kompletnog razvojnog ciklusa u epitelnim ćelijama creva domaćina i izlučenja oocisti fecesom (Hill i sar., 2002). Kod prelaznih domaćina (životinja i ljudi), izostaje enteralni ciklus razvoja. Infekcija kod njih nastaje konzumiranjem mesa prelaznih domaćina koje sadrži tkivne ciste T. gondii sa živim bradizoitima, intrauterino (tahizoitima) i unošenjem sporulisanih oocisti poreklom iz izmeta mačke.
Suština patogenog delovanja T. gondii leži u činjenici da je ona obligatni intracelularni parazit koji se razmnožava u ćelijama gotovo svih organa i tkiva. Dolaskom u ćeliju, paraziti se brzo razmnožavaju i šire se dalje, pri tome stvarajući milijarna nekrotična ognjišta, edeme i formirajući granulaciono tkivo. To za posledicu ima fokalna ili difuzna oštećenja na tim mestima, sa odgovarajućim poremećajima funkcije (Dubey i sar, 2020).
Slika 4. Toxoplasma gondii
Kod goveda se toksoplazmoza manifestuje pobačajima, ali je njen značaj u patologiji neonatalne smrtnosti mnogo manji nego kod ovaca (Kapperud i sar., 1996). Oboljenje je obično praćeno povišenom telesnom temperaturom. Kod goveda se u mleku mogu naći razvojni oblici toksoplazme (tahizoiti), a u muskulautri tkivne ciste (Dubey, 1986). Iz tih razloga, meso i mleko inficiranih životinja predstavljaju izvor infekcije narednih prelaznih domaćina uključujući i čoveka ili prave domaćine (mačke).
Dijagnoza se, kod pravih domaćina (mačaka i drugih felida) postavlja koprološkim pregledom. Kod domaćih životinja se može raditi serološka kontrola, ali se zbog visoke cene analize ne praktikuje nigde u svetu. Namirnice (mleko, meso, jaja) se pregledaju metodom veštačke digestije. Terapija je efikasna samo u akutnoj fazi oboljenja. Mačke se leče klindamicinom p/o 10–40 mg/kg ili i/m 25–50 mg/kg, dok se kod prelaznih domaćina terapija ne sprovodi (Pavlović i Ivanović, 2006).
Sarkocistoza
Sarkocistozu uzrokuju protozoe iz roda Sarcocystis koji obuhvata više vrsta ovih parazita. Razvoj parazita se odvija preko prelaznih domaćina koji se inficiraju ingestijom infektivnih (sporulisanih) sporocista i tkiva sa cistama u kojima se nalaze bradizoiti. Pravi domaćini (ljudi, mačke, psi i divlji mesojedi) se inficiraju samo tkivnim cistama. Kod pravih domaćina se odvija enteroepitelna faza razvoja sa formiranjem oocisti (Dubey i sar. 1989).
Infekcije goveda obično protiču asimptomatski, a od klinčkih simptoma se može pojaviti dijareja. Kod prelaznih domaćina, patogeni efekat je posledica razvoja druge generacije šizonata koja se odvija u endotelu krvnih sudova, što može uzrokovati pobačaje kod gravidnih životinja. Mogu nastati meningoencefalitis, miozitis i limfadenopatija (Gunning i sar., 2000).
U mišićima obolelih životinja (najčešće srčani i skeletni mišići) nalaze se ciste sa bradizoitima (Hornok i sar., 2015)

Slika 5. Sarcocystis sp.
Dijagnostika se kod prelaznih domaćina izvodi serološkim pregledima krvi (test indirektne hemaglutinacije) i nalazom cisti u mišićnom tkivu. Kod pravih domaćina se oociste nalaze tokom koprološkog pregleda. Terapija još nije u potpunosti efikasna, a najbolja je preventiva pregledom mesa koje se koristi u ishrani i njegova adekvatna termička obrada.
Neosporoza
Neosporoza je oboljenje, primarno pasa i goveda, dok su konji, ovce i koze retko inficirani. Uzročnik bolesti je Neospora caninum. Pas je pravi domaćin (mada može biti i prelazni), a prelazni domaćin je goveče (Dubey i sar., 2006). Razvoj neospora je sličan razvoju toksoplazmi.
Infekcija goveda nastaje oocistama neospora preko kontaminirane hrane i vode, a dokazano je i transplacentarno prenošenje. Neospore imaju razvojni put identičan toksoplazmama, uključujući i formiranje tkivnih cisti u mišićima prelaznih domaćina. Klinička slika je u većini slučajeva vezana za abortuse koji se sreću kod 33 procenta inficiranih jedinki (Otter i sar., 1995, Gumber i sar., 2002). Pobačeni plodovi nemaju karakteristične patognomonične lezije (Schares i Conraths, 2007).
Dijagnoza se postavlja histološkim pregledom mozga (ovde se najčešće sreću tkivne ciste), srca i skeletnih mišića fetusa, kao i imunološkim pregledom seruma, što nije u potpunosti pouzdano (Trees i sar., 1994). Ishod terapije je dubiozan i još ne postoji pravi izbor lekova. Najbolje efekte su do sada dali trimetoprim i sulfadiazin.
Literatura:
1. Adamu SG, Adamu NB, Aliyu AU, Atsanda NN, Mustapha FB et al, 2015, Prevalence of Cryptosporidium infection in cattle in Maiduguri, North Eastern Nigeria, Bangl J Vet Med, 13, 1, 25–8.
2. Ahmed WM, Soad EH, 2007, Applied studies on coccidiosis in growing buffalo-calves with special reference to oxidant/antioxidant status, World J Zool, 2, 2, 40–8.
3. Alford CA, Reynolds DW, Stagno S, 1975, Curent conception of chronical prenatal infection, In: Glick L.: Modern Prenatal Medicine, Chicago.
4. Ayinmode AB, Fagbemi BO 2010, Prevalence of Cryptosporidium infection in cattle from South Western infection in cattle from South Western Nigeria, Vet Arch, 80, 6, 723–31
5. Ballweber LR, 2009, Coccidiosis in food animals, In: Smith BP (Eds): Large Animal Internal Medicine. Mosby, Elsevier, St. Louis.
6. Campigotto G, Glombowsky P, Galli GM, Favero JF, da Silva AS, 2017, Gastrointestinal Protozoa in dairy calves: Identification of risk factors for infection, Rev MVZ Cordoba, 22, 2, 5910–24.
7. Dubey JP, 1986, A review of toxoplasmosis in cattle, Vet Parasitol, 23, 3–4, 177–202.
8. Dubey JP, Speer CA, Fayer R, 1989, Sarcocystosis of Animals and Man. Baco Raton, Florida, CRC Press.
9. Dubey JP, Buxton D, Wouda W, 2006, Pathogenesis of bovine neosporosis, J Comp Pathol, 134, 4, 267–89.
10. Dubey JP, Murata FHA, Cerqueira-Cézar CK, Kwok OCH, Yang YR, 2020, Public Health Significance of Toxoplasma gondii Infections in Cattle: 2009–2020, J Parasitol, 106, 6,772–88.
11. Feitosa FLF, Shimamura GM, Roberto T, Mendes LCN, Peiro JR et al, 2008, Importance of Cryptosporidium spp. as a cause of diarrhea in calves, Pesq Vet Brasileira, 28, 10, 452–56.
12. Fitzgerald PR, 1967, Effect of bovine coccidiosis on blood serum sodium and potassium levels of calves, Am J Vet Res.28,667.
13. Fitzgerald PR, 1975, The significance of bovine coccidiosis as a disease in the United States, Bovine Pract, 10, 28.
14. Geurden T, Claerebout E, Vercruysse J, 2005, Protozoan infection causes diarrhea in calves, Tijd Diergen,130, 734–37.
15. Gumber S, Aradhana A, Sharma DR, Singh J, 2002, Neosporosisan emerging cause of bovine abortiona review, Vet Pract,3, 2, 94–100.
16. Gunning RF, Jones JR, Jeffrey M, Higgins RJ, Williamson AG, 2000, Sarcocystis encephalomyelitis in cattle, Vet Rec, 146, 328–31.
17. Heidari H, Dehkordi ZS, Moayedi R, Gharekhani J, 2014, Occurrence and diversity of Eimeria species in cattle in Hamedan Province, Iran Vet Med, 59(6), 271–75.
18. Hill DE, Sreekumar C, Dubey JP, 2002, Toxoplasma gondii, In: Friend M, Brand CJ (Eds.), Field Manual of Wildlife Zoonosis, USGS National Wildlife Health Center, Madison, WI, 357–82.
19. Hornok S, Mester A, Takács N, Baska F, Majoros G et al, 2015, Sarcocystis-infection of cattle in Hungary, Paras Vec, 8, 69.
20. Hunter PR, Thompson RCA, 2005, The zoonotic transmission of Giardia and Cryptosporidium, Int J Parasitol, 35, 1181–90.
21. Kapperud G, Jenum PA, Stray-Pedersen B, Melb KK, Eskil A et al, 1996, Risk factors for Toxoplasma gondii infection in pregnancy, Results of a prospective case-control study in Norway, Am J Epidemiol, 144, 405–12.
22. Marskole P, Verma Y, Dixit AK, Swamy M, 2016, Prevalence and burden of gastrointestinal parasites in cattle and buffaloes in Jabalpur, India Vet World, 9, 11, 1214–17.
23. Olson ME, O’Handley R, Ralston B, Thompson RCA, 2004, Emerging issues of Cryptosporidium and Giardia infections in cattle, Tren Parasitol, 20, 185–91.
24. Otter A, Jeffrey M, Griffiths IB, Dubey JP, 1995, A survey of the incidence of Neospora caninum infection in aborted and stillborn bovine fetuses in England and Wales, Vet Rec, 136, 602–06.
25. Pavlović I, Ivanović S, 2006, Toksoplazmoza, Naučni institut za veterinarstvo Srbije i Ministarstvo poljoprivrede, šumarstva i vodoprivrede, Beograd.
26. Pavlović I, Rogožarski D, 2017, Parazitske bolesti domaćih životinja sa osnovima parazitologije i dijagnostike parazitskih bolesti, Naučna KMD, Beograd.
27. Schares G, Conraths FJ, 2007, Neospora caninum as a cause of bovine abortionnews regarding pathogenesis, epidemiology and diagnosis, Prakt Tierarzt, 88, 9, 730–40.
28. Sevinc F, 2004, Cryptosporidiosis in ruminants. Vet Bilim Dergisi, 20, 4 , 79–84.
29. Soltane R, Guyot K, Dei-Cas E, Ayadi A, 2007, Prevalence of Cryptosporidium spp. (Eucoccidiorida: Cryptosporidiidae) in seven species of farm animals in Tunisia, Parasite, 14, 4, 335–8.
30. Szostakowska B, Lozowska WK, Racewicz M, Knight R, Tamang L et al, 2004, Cryptosporidium parvum and Giardia lamblia recovered from flies on a cattle farm and in a landfill, Appl Environ Microbiol, 70, 6, 3742–44.
31. Taylor MA, Webster KA, 1998, Recent advances in the diagnosis of Cryptosporidium, Toxoplasma, Giardia and other protozoa of veterinary importance, Res Vet Sci, 65, 183–93.
32. Teankum K, Pirarat N, Moungyai M, 2003, Eimeria zuernii infection in Thai native calves, Thai J Vet Med, 33, 2, 114–8.
33. Thomas HS, 1994, Coccidiosis in calves, The Cattleman, 81, 21–32.
34. Trees AJ, Guy F, Low JC, Roberts L, Buxton D, Dubey JP, 1994, Serological evidence implicating Neospora species as a cause of abortion in British cattle, Vet Rec, 134, 405–07.
35. Taylor M, 2000, Protozoal disease in cattle and sheep, In Practice, 22, 604–17.
36. Yatoo MI, Melepad DP, Dimri U, 2013, Coccidiosis in buffalo calf: a case report, Res J Vet Pract, 1, 4, 46–72.
37. Xiao L, Herd RP, 1994, Infection pattern of Cryptosporidium and Giardia in calves, Vet Parasitol, 55, 257–62.