 Udruženje vetrinara praktičara Srbije - UVPS
Udruženje vetrinara praktičara Srbije - UVPS
Terapija kompleksa cistična endometrijalna hiperplazija – piometra
Autor:
Prof. dr sc. vet. med. Vladimir Magaš - Fakultet veterinarske medicine, Univerzitet u Beogradu, Katedra za porodiljstvo, sterilitet i veštačko osmenjavanje
Kratak sadržaj: Kompleks cistična endometrijalna hiperplazija — piometra (CEH-P kompleks) je reproduktivni poremećaj koji je veoma čest, uglavnom kod starijih kuja nakon estrusa. U nastajanju ovog poremećaja, jednu od glavnih uloga ima fiziološki efekat progesterona na matericu. Poremećaj se pojavljuje i sa otvorenim i sa zatvorenim cerviksom, a često utiče na opšte stanje pacijenta. Detaljna anamneza, opšti i specijalistički klinički pregled, uz nezaobilaznu ultrasonografsku dijagnostiku, su osnova za pravilnu procenu i prognozu, izbor terapije i izlečenje. U terapiji CEH-P kompleksa postoje dva pristupa lečenju. Tradicionalni hirurški pristup je i dalje zlatni standard u terapiji ovog, ne retko fatalnog, reproduktivnog problema i podrazumeva ovariohisterektomiju. Konzervativni pristup, ali i prehirurški tretman, zahtevaju agresivnu simptomatsku terapiju, pre svega tečnostima i antibioticima uz istovremenu primenu specijalne terapije koja uključuje upotrebu steroidnih antiprogesteronskih preparata ili dopaminskih agonista, prirodnih prostaglandina ili njihovih analoga, uterotonika ili relaksanasa miometrijuma, zavisno od procene veterinara. Prednost hirurškog tretmana je istovremeno uklanjanje purulentnog sadržaja i prevencija oslobađanja toksina, dok su nedostaci: rizici od anestezije i ireverzibilani sterilitet. Kod lošeg opšteg stanja pacijenta, visoko vrednih priplodnih jedinki, ali i kod pripreme rizičnih pacijenta za hirurški tretman, savetuje se konzervativni pristup. Jedan od efikasnijih protokola uključuje kombinaciju antiprogesteronskog preparata aglepristona i prirodnog prostaglandina. Individualizacija svakog pacijenta na osnovu anamneze i dijagnostičkih nalaza treba da bude osnova za odabir terapije u lečenju CEH-P kompleksa i najbolji ishod.
Ključne riječi: aglepriston, CEH, dopaminski agonisti, piometra, prostaglandini
Uvod
Piometra se kod kuja i mačaka definiše kao akumulacija purulentnog sadržaja u materici i pojavljuje se ili sa otvorenim (otvorena piometra) ili zatvorenim (zatvorena piometra) cerviksom. Kod starijih kuja, piometra se najčešće pojavljuje u periodu estrusa, a ređe i neposredno nakon njega, odnosno u metestrusu. Poslednjih godina, zapažena je sve je češća pojava ovog oboljenja i kod mlađih intaktnih jedinki, ali i kuja koje su se štenile, uz izvesnu rasnu predispoziciju. U reproduktivnoj patologiji kuja postoji i CEH (engl. cystic endometrial hyperplasia – CEH) ili takozvani "CEH-P complex" koji se definiše kao oboljenje supkliničkog toka koje karakteriše proliferacija endometrijalnih žlezdi od kojih nastaju ciste ispunjene tečnošću sa prisustvom sadržaja u lumenu materice (Batista i sar., 2016). U najvećem broju slučajeva, kod kuja sa CEH, posledično nastaje i piometra. Tačna etiologija nastanka ova dva povezana oboljenja (sindrom) je još nepoznata, ali se kategoriše kao ozbiljna bakterijska infekcija sa značajnom ulogom endokrinog sistema. Dokazano je da ne postoji veza između broja partusa ili karakteristika estrusnog ciklusa na nastanak kompleksa CEH — piometra (Verstegen i sar., 2008). Piometra je bolest lutealne faze, tako da se kod kuja najčešće pojavljuje od 5. do 80. dana, od kraja estrusa. Hormon koji ima glavni uticaj na nastanak CEH je progesteron. U toku fiziološkog polnog ciklusa kuje, pod uticajem progesterona, nastaje kontinuirana endometrijalna hiperplazija i glandularna sekrecija koja regresira na kraju lutealne faze. Kod kuja ne postoji period menopauze. Tokom života kuje, glandularna hiperplazija ima progresivan tok koji na kraju rezultira razvojem patoloških promena (lezija) u vidu cistične endometrijalne hiperplazije. Serumske koncentracije estrogena i progesterona nisu promenjene i sumnja se da povećan broj i osetljivost hormonskih receptora iniciraju nastanak CEH (Hagman, 2017).
Kod mačaka, piometra nije tako učestalo oboljenje zbog prirode polnog ciklusa (sezonalnost, indukovana ovulacija) i manjeg uticaja progesterona. Javlja se kod svega 2,2 procenta mačaka pre 13 godina starosti (Misk i El-Sherry, 2020).
Bakterije koje se najčešće mogu izolovati iz materice u slučaju piometre su E. coli, Staphylococcus aureus, Streptococcus spp., Pseudomonas spp. i Proteus spp. Međutim i kod zdravih kuja, vaginalnu floru čine upravo navedeni mikroorganizmi (Watts, 1996). U najvećem broju slučajeva, preovlađuje E. coli, koja preko uropatogenog faktora virulencije (UVF) nalazi mesta za vezivanje u endometrijumu stimulisanom progesteronom.
Dijagnostika, prognoza i ishod — faktori rizika
Piometra i CEH su potencijalno opasni po život jedinke sa dužom listom komplikacija koja uključuje sepsu, septični šok, peritonitis, diseminiranu bakterijsku infekciju i posledičnu disfunkciju više organa (Fransson i sar., 2004). Povoljan ishod se može očekivati samo pravovremenom dijagnostikom i odgovarajućom terapijom. Kod jedinki kod kojih je izvršen adekvatan hirurški tretman, prijavljen je samo jedan procenat uginuća (1%). Kao najčešća komplikacija se navodi peritonitis i to u 10 procenata slučajeva. Na osnovu ispitivanja prediktivnih faktora, zaključeno je da su leukopenija i abnormalna telesna temperatura (niska ili visoka) ispoljile najveću povezanost sa nastankom peritonitisa (Jitpean i sar., 2014).
Kod klasičnih slučajeva CEH-piometre sa otvorenim cerviksom, dijagnostika je olakšana. Slučajevi kod kojih je cerviks zatvoren, a klinička slika bez vidljivih signifikantnih promena, se značajno teža dijagnostikuju. U takvim situacijama se treba osloniti na detaljnu anamnezu (poslednji estrus), klinički pregled, hematološke i biohemijske analize krvi i nezaobilaznu ultrazvučnu/radiološku dijagnostiku. Palpacijom abdomena se u nekim slučajevima može detektovati uvećan uterus, ali pregled treba raditi veoma pažljivo zbog rizika od rupture (Batista i sar., 2015).
Slučajevi piometre su uglavnom praćeni izrazitom leukocitozom koju karaterišu neutrofilija sa skretanjem u levo i toksična degeneracija neutrofilnih granulocita, kao i monocitoza. Međutim, oni nisu uvek prisutni, s obzirom na činjenicu da se u 25 procenata slučajeva piometre leukogram nalazi u fiziološkim granicama. Mnoge obolele kuje imaju blagu do umerenu normocitno normohromnu anemiju (Hct 30–35%) koja odražava hroničnu prirodu bolesti i toksičnu aplaziju ili hipoplaziju kostne srži. Procena anemije je često komplikovana istovremenom dehidratacijom. Jedan od pouzdanih parametara biohemijskih analiza krvi je povišena aktivnost serumske alkalne fosfataze (AP), koja je nalaz u oko 50–75 procenata slučajeva. Povremeno se aktivnost serumske alanin aminotransferaze takođe može blago povećati (Verstegen i sar., 2008). Povećana serumska aktivnost AP ukazuje na hepatocelularna oštećenja kao odgovor na toksemiju ili smanjenu cirkulaciju krvi u jetri zbog dehidratacije. Hiperproteinemija se može razviti kao odgovor na dehidrataciju, a hiperglobulinemija odražava hroničnu antigensku stimulaciju prisutnu kod ove bolesti (Arora, 2007).
Kao česta komplikacija kod piometre kuja, navodi se bubrežna disfunkcija. Koncentracije azotnih jedinjenja, pre svega uree i kreatinina u serumu obično nisu povišene, osim ako se ne razvije prebubrežna azotemija kao posledica dehidratacije. Kod hirurški lečenih životinja, azotemija se obično brzo razrešava nakon agresivne terapije tečnostima i operativnog zahvata, potvrđujući prerenalnu prirodu azotemije. Azotemija je uglavnom povezana sa težom kliničkom slikom. Čak i kod neazotemijskih rehidriranih pacijenata, glomerularna filtracija se obično smanjuje, što ukazuje na to da neki faktori povezani sa bolešću utiču na bubrežnu perfuziju bilo u prisustvu ili odsustvu azotemije (Hagman, 2017).
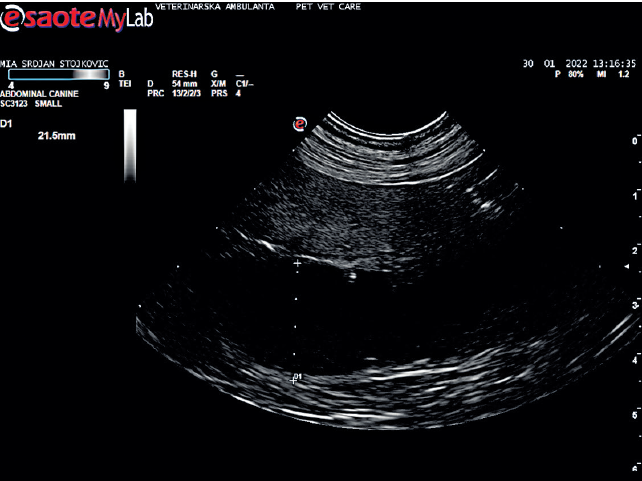
Slika 1. CEH — kolekcija gustog gnojnog sadrzaja nakon dvodnevne konzervativne terapije pre hirurske intervencije, rotvajler Mia, 11 godina
U nekim slučajevima je zapažena infekcija urinarnog trakta istim mikroorganizmom koji inficira matericu (obično E. coli). Cistocenteza se u tim situacijama ne preporučuje, zbog velikog rizika od perforacije dilatirane materice. U ranoj fazi bolesti, specifična težina mokraće je promenljiva i često je u graničnom opsegu. Smatra se da endotoksini E. coli imaju specifičnu sposobnost da izazivaju tubularnu neosetljivost na antidiuretički hormon, izazivajući sekundarni nefrogeni diabetes insipidus. Ovo rezultira daljim gubitkom koncentracione sposobnosti bubrega i dovodi do poliurije i kompenzatorne polidipsije (Arora, 2007).
Insuficijencija bubrega i gubitak proteina mokraćom nisu uobičajena pojava, međutim, kod nekih kuja, piometra može dovesti do trajnog otkazivanja bubrega. Ovaj podatak dokazuje važnost praćenja proteinurije kao dragocenog prognostičkog indikatora u postoperativnom monitoringu kuja sa piometrom (Verstegen i sar., 2008).
Radiografski snimak kod piometre potvđuje prisustvo uvećane tubularne strukture u kaudoventralnom delu abdomena. Ultrazvučni pregled ima nesumnjivu prednost u detekciji sadržaja u materici, posebno kada je dijametar materice u normalnim okvirima, ali i u detekciji dodatnih patoloških promena u tkivu materice i jajnika, kao što su cistične promene kod CEH piometre (Magaš i sar., 2016).
Terapija
Tradicionalni pristup lečenju piometre je hirurški tretman i podrazumeva uklanjanja jajnika i materice (ovariohisterektomija — OHE), pri čemu se istovremeno uklanja i purulentni sadržaj i prevenira oslobađanje toksina. Nedostaci hirurškog pristupa su rizik od uvođenja jedinke u anesteziju i ireverzibilni sterilitet. Može se reći da je ovariohisterektomija preporučeni vid terapije, posebno za kuje bez značajne reproduktivne vrednosti ili kada vlasnik ne želi da se kuja ponovo pari (Fieni i sar., 2014).
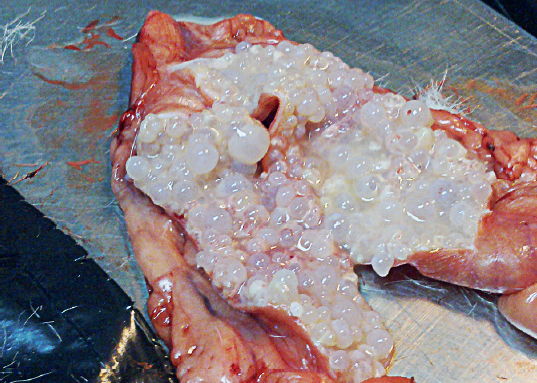
Slika 2. CEH — Cystic Endometrial Hyperplasia — materica sa izraženim cistama
Zbog prirode ovog oboljenja i ponekad kontroverzne kliničke slike, pacijenti su neretko u lošem stanju koje povećava rizike od anestezije i otežava izvođenje operacije. Lečenje ne treba previše odlagati, ali se pacijenti moraju stabilizovati pre hirurške intervencije, intravenskom nadoknadom tečnosti i antibioticima širokog spektra. Obavezno treba proceniti funkciju bubrega i jetre i postupati prema tome. Potpornu i antibiotsku terapiju treba nastaviti tokom operacije i još najmanje nedelju dana nakon hirurške intervencije. Uprkos ovim merama predostrožnosti, neke komplikacije se ipak mogu javiti. Glavna prednost OHE je isključenje bilo kakvog recidiva. Međutim, hirurški pristup ima svoja ograničenja, pogotovo kada postoje rizici od anestezije i komplikacije u toku i posle hirurškog zahvata (krvarenja, ruptura materice, DIC), a naročito kod pacijenata u lošem opštem stanju.
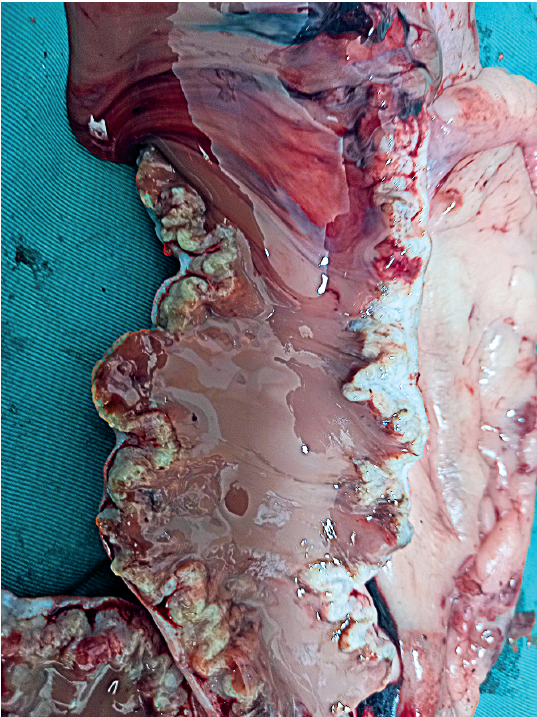
Slika 3. Piometra sa gnojnim sadržajem i cistama
Konzervativni (medikamentozni) pristup je indikovan kod:
- Priplodnih kuja;
- Kuja u lošoj kondiciji ili starih kuja, hipo i hipertermičnih kuja, kod prevelikog rizika od anestezije;
- Slučajeva kada vlasnici žele najmanje troškove lečenja;
- Poboljšanja opšteg zdravstvenog stanja kuje pre hirurškog tretmana.
Konzervativni pristup je kontraindikovan kod pacijenata sa sumnjom na peritonitis. Efikasnost medikamentozne terapije zavisi od kliničke slike: metritis, otvorena ili zatvorena piometra, prisustvo ili izostanak ovarijalnih cisti. Konzervativna terapija podrazumeva opšti i specifični tretman (Fieni i sar., 2014).
U opštu terapiju spada sprovođenje protokola bez obzira na dalji tok lečenja i ona uključuje:
- Stavljanje elizabetanske kragne u cilju preveniranja lizanja i ingestije vulvarnog iscetka;
- Antibiotsku terapiju bez korišćenja nefrotoksičnih preparata (npr. amoksicilin-klavulanska kiselina 25 mg/kg/dan) u cilju preveniranja septikemije kod pacijenata sa lošim opštim stanjem ili kod onih kuja gde monitoring nije moguć i
- Intravensku nadoknadu tečnosti (60 ml/kg + % dehidracije × telesna težina/100) u cilju preveniranja dehidratacije i toksičnog šoka.
Specifični tretman podrazumeva upotrebu prostaglandina, dopaminskih agonista i antiprogestina. U terapiji piometre se koriste ponavljajuće doze prostaglandia F2α (PGF2α) koji ima luteolitičko i uterotonično dejstvo. Indikacije za upotrebu PGF2α su terapija metritisa i otvorene piometre kod "zdravih" kuja (mladih) sa normalnom funkcijom bubrega i jetre, bez hipertrofije uterusa. Redukcija koncentracije progesterona izaziva relaksaciju cerviksa, smanjenje sekretorne aktivnosti endometrijuma i pojačanu evakuaciju sadržaja. Međutim, kada se koriste visoke doze, prostaglandini su takođe povezani sa znatnim rizikom od rupture materice, posebno u slučajevima piometre sa zatvorenim grlićem (Fieni i sar., 2014). Visoke doze prostaglandina se dovode u vezu sa značajnim neželjenim i štetnim efektima, uključujući pojačanu salivaciju, povraćanje, naprezanje, dijareju, pireksiju, neke povremene respiratorne tegobe kao i sa pojedinačnim slučajevima šoka i smrti. U slučajevima zatvorene piometre, upotreba PGF2α je ponekada povezana sa nastankom peritonitisa, praćenog odlivom purulentnog sadržaja ascedentnim putem ka jajovodu, ovarijalnoj burzi i peritoneumu (Fieni i sar., 2014).
Preporučeno trajanje tretmana sa jednokratnom dnevnom administracijom PGF2α, je 5–7 dana sa 0,25 mg/kg prirodnog PGF2α ili 10 μg/ kg kloprostenola (Fieni i sar., 2014). Drugi pristup je terapija prirodnim PGF2α u dozama od 10–50 µg/kg, tri do pet puta dnevno tokom 3–7 dana, bilo pojedinačno ili u kombinaciji sa drugim preparatima.
Efikasnost odabranog protokola se proverava ultrazvučnim pregledom najbolje svakodnevno, a obavezno nakon 10–14 dana. Po potrebi je moguće i ponoviti tretman. Kod 15 procenata lečenih kuja, analizom krvi je ustanovljena septikemija i zbog toga je od izuzetne važnosti preventivna sistemska antibiotska terapija (Feldman i Nelson, 2004).
Prirodni prostaglandini su poželjniji od analoga prostaglandina, ne samo zbog toga što izazivaju luteolizu, već njihova primena rezultira i značajnijim kontrakcijama materice. Posebnu pažnju treba obratiti na dozu s obzirom na to da je terapeutska širina relativno mala (L D50 kod pasa je oko 5 mg/kg), a nuspojave su prilično ozbiljne kada se koriste visoke doze analoga (>10 µg/kg). Aplikacija leka se najčešće vrši supkutano. Kako su neželjeni efekti dozno zavisni, preporučuje se da se započne sa najmanjom dozom (često i subdozirati) kako ne bi došlo do ozbiljnih neželjenih efekata, a zatim postepeno povećavati dozu.
Postoje različite tehnike aplikacije u cilju smanjenja neželjenih efekata PGF2α:
- Aplikacija progresivnih doza PGF2α: 1. dan 0,1 mg/kg, 2. dan 0,2 mg/kg i nastaviti sa 0.25 mg/kg (Feldman i Nelson, 2004);
- Aplikacija PGF2α pre hranjenja;
- Pretretman — npr. atropin pre aplikacije PGF2α.
Intravaginalna infuzija prirodnih prostaglandina, jednom ili dva puta dnevno, je takođe dala dobre rezultate i to bez nuspojava (Gábor, 1999). Aplikaciju prostaglandina treba izbegavati kao vid terapije piometre kod brahiocefaličnih rasa (specijalno engleskih buldoga) zbog toga što su kod njih nuspojave znatno izraženije i mogu dovesti do ozbiljnih komplikacija pa i do smrti.
Najvažniji luteotropni hormon kod kuja je prolaktin, a višekratna primena inhibitora prolaktina od 25. dana nakon ovulacije, dovodi do brzog i trajnog smanjenja koncentracije progesterona u krvnoj plazmi (Onclin, 1994), što je efekat koji se koristi i za indukciju arteficijalnog abortusa. U novije vreme, inhibitori prolaktina se kombinuju sa niskim dozama prostaglandina za lečenje piometre u pokušaju da se ubrza luteoliza, što je ranije potvrđeno kod indukcije pobačaja (Onclin, 1999).
Dopaminski agonisti, kao što su bromokriptin ili kabergolin, sa značajnim anti-prolaktinskim efektom, se koriste u kombinaciji, bilo sa prirodnim ili sa sintetskim prostaglandinima (Tabela 1). Kabergolin je obično prvi izbor, s obzirom na to da ima manje nuspojava i može se primenjivati samo jednom dnevno u odnosu na dva ili tri puta dnevno preporučenu aplikaciju bromokriptina. Kombinacija agonista dopamina i prostaglandina potencira luteolitičke efekte i rezultira bržom luteolizom (Onclin,1999). Kada se koristi kombinacija ovih terapeutika, koncentracija progesterona u serumu opada za <24 do 48 h, dok će male doze samo prostaglandina ispoljiti svoje efekte tek posle 3–4 dana.
Aglepriston spada u antiprogestine i kompetetivno se vezuje za progesteronske receptore pa time umanjuje intrauterinu koncentraciju i dejstvo progesterona. Inicijalno, aglepriston je korišćen za izazivanje arteficijalnog abortusa i indukciju porođaja. Njegov mehanizam dejstva se koristi i u terapiji piometre (Jurka i sar., 2010).
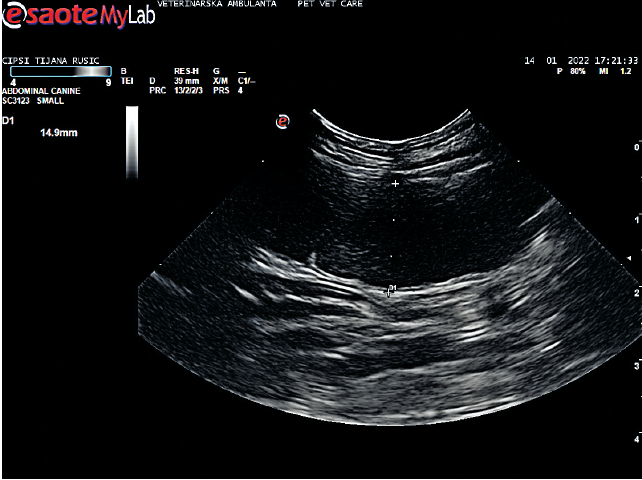
Slika 4. Ehonogram materice sa piometrom pre terapije
Tabela 1. Doziranje dopamiskih agonista u terapiji piometre.
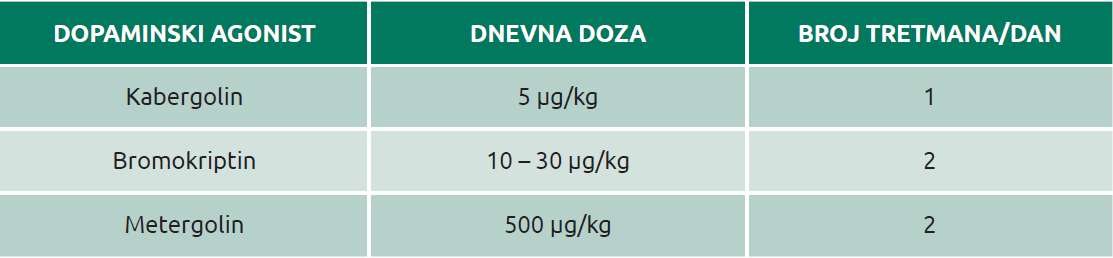
Preuzeto iz: Romagnoli, 2006.
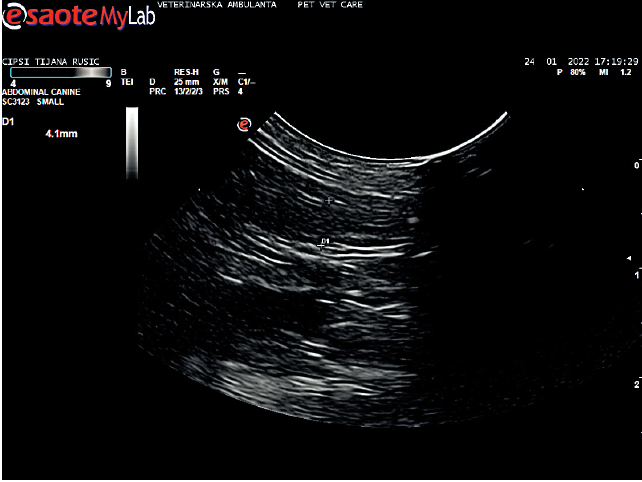
Slika 5. Ehonogram materice sa posle konzervativne terapije
U literaturi se navodi više protokola za upotrebu aglepristona, a jedan od najefikasnijih je supkutana aplikacija 10 mg/kg aglepristona jednom dnevno, i to 1., 2., i 8. dana. Ukoliko se posle tretmana, na ultrazvučnom pregledu i dalje vizuelizuje lumen materice, neophodno je aplikovati još jednu dozu 15. dana (Fieni, 2006). Kada je lumen materice potpuno ispražnjen, terapija se završava. U cilju poboljšanja efekta terapije aglepristonom, može se dodati sintetski analog kloprostenol u dozi od 1 μg/kg sc kada se postiže snažnije uterotonično i luteolitičko dejstvo (Fieni i sar., 2014).
Zaključak
Nakon početne agresivne simptomatske terapije tečnostima i antibioticima, u izboru daljeg protokola lečenja treba biti izuzetno pažljiv, a terapija CEH-P kompleksa treba da bude individualna i na osnovu pomenutih kliničkih i dijagnostičkih nalaza.
U terapiji metritisa i zatvorene piometre, sintetski steroidni antiprogestagen aglepriston je efikasan i izaziva otvaranje cerviksa. Kombinacija odgovarajućih doza sintetskih analoga prostaglandina ili prirodnog PGF2α sa antiprogestagenom aglepristonom ili inhibitorima prolaktina daje izuzetno dobre efekte u terapiji zatvorene i otvorene piometre.
Literatura:
1. Arora N, 2007, Role of uropathogenic virulence factors in the pathogenesis of E. coli-induced cystic endometrial hyperplasia/pyometra complex in the bitch, PhD thesis, University of Melbourne Australia, 250.
2. Batista PR, Gobello C, Rube A, Corrada YA, Tórtora M, Blanco PG, 2016, Uterine blood flow evaluation in bitches suffering from cystic endometrial hyperplasia (CEH) and CEH-pyometra complex, Theriogenology, 85, 1258–61.
3. Feldmann EC, Nelson RW, (eds), 2004, Cystic endometrial hyperplasia/pyometra complex. In: Canine and Feline Endocrinology and Reproduction, 3rd ed. WB Saunders Co, Philadelphia, PA, 852–67.
4. Fieni F, 2006, Clinical evaluation of the use of aglepristone to treat cystic endometrial hyperplasia-pyometra complex in bitches, Theriogenology 66, 1550–6.
5. Fieni F, Topie E, Gogny A, 2014, Medical treatment for pyometra in dogs. Reprod Dom Anim, 49, 28–32.
6. Fransson BA, Karlstam E, Bergström A, Park JS, Evans MA, Ragle CA, 2004, C -reactive protein in the differentiation of pyometra from cystic endometrial hyperplasia/mucometra in dogs, JAAHA, 40, 391–9.
7. Gabor G, Siver L, Szenci O, 1999, Intravaginal prostaglandin F2 alpha for the treatment of metritis and pyometra in the bitch, Acta Vet Hung, 47, 103–8.
8. Hagman R, 2017, Canine pyometra: What is new?, Reprod Dom Anim, 52, 288–92.
9. Jitpean S, Ström-Holst B, Emanuelson U, Höglund OV, Petersson A, Alneryd-Bull C, Hagman R, 2014, Outcome of pyometra in female dogs and predictors of peritonitis and prolonged postoperative hospitalization in surgically treated cases, BMC Vet Res, 10, 6.
10. Jurka P, Max A, Hawrynska K, Snochowski M, 2010, Age related pregnancy results and further examination of bitches after aglepristone treatment of pyometra. Reprod Dom Anim, 45, 525–9.
11. Magaš V, Nedić S, Stanišić Lj, Pavlović M, Vakanjac S, 2016, Primena ultrazvuka u reprodukciji domaćih životinja, Zbornik predavanja, 7. naučni simpozijum "Reprodukcija domaćih životinja" 6–9. okt. 2016, Divčibare, Srbija, 93–104.
12. Misk TN, El-Sherry TM, 2020, Pyometra in Cats: Medical Versus Surgical Treatment, J Curr Vet Res, 2, 86–92.
13. Onclin K, Silva LD, Donnay I, Verstegen JP, 1994, Luteotrophic action of prolactin in dogs and the effects of a dopamine agonist, cabergoline. J Reprod Fertil, 47, 403–9.
14. Onclin K, Verstegen JP, 1999, Comparisons of different combinations of analogues of PGF2 alpha and dopamine agonists for the termination of pregnancy in dogs. Vet Rec, 144, 416–9.
15. Prasad VD, Kumar PR, Sreenu M, 2018, Pyometra in bitches: a review of literature, J Vet Sci Tech, 6, 12–20.
16. Romagnoli S, 2006, Control of reproduction in dogs and cats: use and misuse of hormones. In World Congress WSAVA/FECA/CSAVA.
17. Sethi GPS, Gandotra VK, Honparkhe M, Singh AK, Arora AK, Ghuman SPS, 2020, Efficacy of Antiprogesterone and PGF2α Therapy for Treating Canine Pyometra, Int J Curr Microbiol App Sci, 9, 2117–23.
18. Verstegen J, Dhaliwal G, Verstegen K, 2008, Mucometra, cystic endometrial hyperplasia, and pyometra inthe bitch: Advances in treatment and assessment of future reproductive success, Theriogenology, 70, 364–74.