 Udruženje vetrinara praktičara Srbije - UVPS
Udruženje vetrinara praktičara Srbije - UVPS
Veštačko osemenjavanje kobila zamrznutim semenom
Autor:
Dr sc. vet. med. Saša Lauš - VA ZOOMEDICA, Pavliš
Kratak sadržaj: Danas se u reprodukciji konja sve više koriste metode asistirane reprodukcije. Veštačko osemenjavanje kobila postaje sve popularnije, a u poslednjih tridesetak godina je prihvaćeno od strane mnogih odgajivačkih organizacija. Tehnika zamrzavanja semena i tehnika osemenjavanja su poboljšane, a procenat ždrebnih kobila je gotovo isti kao i pri korišćenju svežeg ili rashlađenog semena. Osemenjavanje kobila zamrznutim semenom zaheva veći broj pregleda, kako bi se seme unelo tačno u određenom mometu polnog ciklusa kobile.
Pre osemenjavanja, treba proveriti da li je kobila dobar kandidat za VO zamrznutim semenom, primenjujući rutinske preglede reproduktivnog trakta koje mogu da uključe mikrobiološki i citološki pregled brisa kada je to indikovano.
Da bi se predvidelo vreme ovulacije i odredilo optimalno vreme osemenjavanja zamrznutim semenom, koriste se hCG ili deslorelin. Tehnika dubokog intrakornualnog osemenjavanja obuhvata korišćenje specijalnog dugog katetera, koji se rektalnom manipulacijom uvodi u vrh roga, ipsilateralno sa jajnikom na kome je ovulirao folikul. Kobilu je potrebno pregledati 18–24 časa nakon osemenjavanja da bi se isključilo prisustvo tečnosti u materici. Procenat ždrebnih kobila po ciklusu je od 30 do 70.
Ključne reči: kobile, veštacko osemenjavanje, zamrznuto seme
Danas se u reprodukciji konja sve više koriste metode asistirane reprodukcije. Asistirana reprodukcija datira još od kraja devetnaestog veka kada je dobijen prvi graviditet metodom veštačkog osemenjavanja.
Pored veštačkog osemenjavanja, kao metoda asistirane reprodukcije u reprodukciji konja, se najčešće koristi embriotransfer. Pojedina grla nisu u stanju da stvore embrion zbog patoloških promena na reproduktivnim organima. Takođe i vrlo vredni pastuvi nisu uvek u stanju da daju potomstvo prirodnim pripustom ili veštačkim osemenjavanjem. Zbog toga su razvijene druge metode proizvodnje embriona in vivo i in vitro. U ove metode spadaju:
- Transfer oocita
- Intracitoplazmatična injekcija spermatozoida (ICIS)
- In vitro fertilizacija
- Intrafalopijalni transfer gameta (GIFT)
- Kloniranje ?
Veštačko osemenjavanje kobila
Od svih prethodno nabrojanih metoda asistirane reprodukcije, u rutinskoj praksi se najčešće izvodi veštačko osemenjavanje, a u poslednje vreme i embriotransfer.
Veštačko osemenjavanje je unošenje odgovarajućeg broja spermatozoida u matericu zdrave kobile u odgovarajuće vreme. Prvi organizovani programi veštačkog osemenjavanja kobila su pokrenuti na ruskim ergelama. U poslednjih tridesetak godina, veštačko osemenjavanje je prihvaćeno od strane mnogih nacionalnih i internacionalnih odgajivačkih organizacija širom Evrope, Amerike i Australije. U nekim zemljama, kao što su Holandija, Francuska i Italija, svake godine se osemeni nekoliko hiljada kobila. Uspeh ili neuspeh programa veštačkog osemenjavanja, u velikoj meri zavisi od menadžmenta koji je vezan za reprodukciju. Pre svega tu spadaju: metod i vreme veštačkog osemenjavanja, kvalitet semena i pravilno rukovanje semenom, kao i pregledi kobila i intervencije pre i nakon ovulacije. Za uspešnu reprodukciju kobila neophodan je stalni nadzor veterinara. Osemenjavanje kobila zamrznutim semenom je vrlo dugo bilo zanemareno kao komplikovan proces koji oduzima puno vremena, koji daje loše rezultate i ima za posledicu velike račune od strane veterinara. U poslednjih dvadesetak godina, tehnike zamrzavanja semena i tehnike osemenjavanja su značajno poboljšane, a procenat gravidnih kobila je gotovo isti kao i kod korišćenja svežeg ili rashlađenog semena.
Prednosti i nedostaci veštačkog osemenjavanja zamrznutim semenom
Prednosti VO kobila zamrznutim semenom su:
1. Izbegavanje stresa zbog transporta kobile (i ždrebeta);
2. Racionalno iskorišćavanje semena (od jednog ejakulata se može osemeniti više kobila);
3. Dostupnost semena vrednih pastuva iz celog sveta;
4. Mogućnost čuvanja semena godinama;
5. Smanjena mogućnost povrede kobile ili pastuva prilikom pripusta;
6. Sprečavanje prenošenja polno prenosivih bolesti i drugih bolesti i
7. Mogućnost korišćenja zamrznutog semena i nakon uginuća pastuva (ovo zavisi od odgajivačke asocijacije, naime seme pastuva kasača se ne može koristiti nakon uginuća pastuva).
Nedostaci VO kobila zamrznutim semenom su sledeći:
1. Seme nekih pastuva se ne može zamrzavati;
2. Neke odgajivačke organizacije ne dozvoljavaju veštačko osemenjavanje kobila i
3. Zbog potrebe češćih kontrola i prisustva veterinara, cena osemenjavanja zamrznutim semenom je veća.
Izbor kobila za veštačko osemenjavanje zamrznutim semenom
Na uspeh veštačkog osemenjavanja kobila utiču brojni faktori. Jedan od važnih faktora je starost kobila koje osemenjavamo i najbolji rezultati se postižu kod kobila koje su stare između 4 i 12 godina. Reproduktivni status kobila je takođe veoma važan faktor pri izboru kobila koje ćemo osemenjavati. Prema reproduktivnom status, kobile se mogu podeliti na: (1) kobile koje se prvi put uvode u reprodukciju — nikada ranije nisu osemenjene svežim, rashlađenim, zamrznutin semenom ili prirodno parene; (2) oždrebljene kobile — kobile koje imaju ždrebe u sezoni u kojoj se osemenjavaju; (3) jalove kobile — kobile koje u prethodnoj ili nekoliko prethodnih sezona nisu ostajale ždrebne.
Rezultati su donekle bolji kod oždrebljenih kobila (54 procenta), nego kod onih koje se prvi put uvode u reprodukciju (35 procenata) ili kod jalovih (53 procenta). Slabiji rezultati se dobijaju ako se kobile osemene u ždrebećem estrusu (manja koncepcija i povećan embrionalni mortalitet), tako da kobile ne bi trebalo osemenjavati u ovom prvom estrusu nakon ždrebljenja, mada nije svejedno da li kobila ovulira 8–9 dana nakon porođaja ili se to desi nakon 14–15 dana.
Pregled kobila pre uvođenja u veštačko osemenjavanje
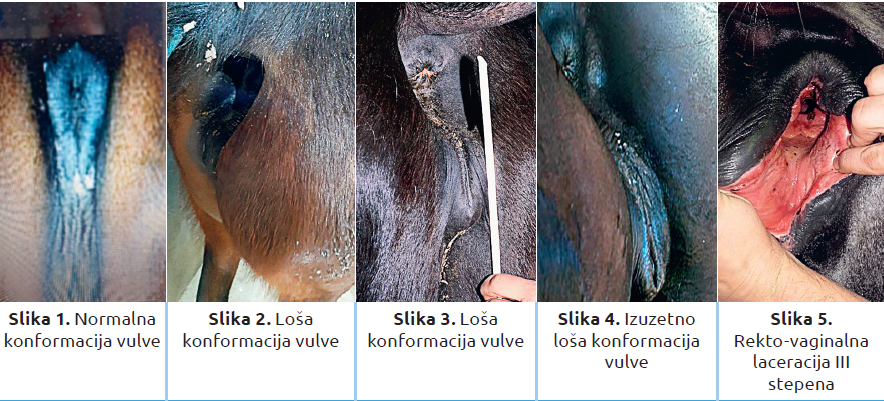
Kobile koje dođu na veštačko osemenjavanje prvo treba pregledati. Oceniti fizičku kondiciju i uraditi klinički pregled i proveriti vakcinacije. Prekomerno debele (gojazne) kobile češće imaju metaboličke probleme, kao PPID (disfunkcija intermedijernog režnja hipofize). S druge strane, mršave kobile teže ulaze u estrus. Takođe treba pregledati i perinealnu regiju i utvrditi da li postoje povrede, kakva je konformacija vulve i da li postoji iscedak iz vagine (slike 1–5). Vulva, vestibulovaginalni sfinkter i cerviks su barijere od kontamicije vazduhom i fecesom.
Nakon ovog pregleda, treba uraditi pregled reproduktivnog trakta rektalnom palpacijom čime utvrđujemo veličinu, tonus i položaj materice, simetriju materičnih rogova, stanje cerviksa i jajnika.
Ultrazvučni pregled
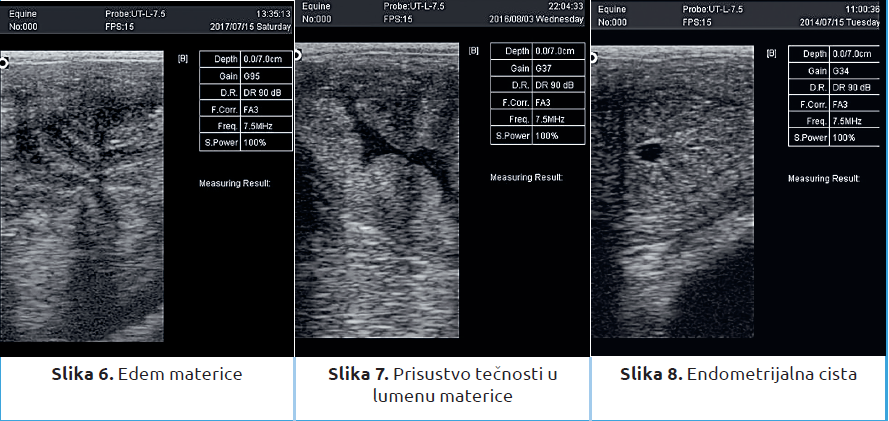
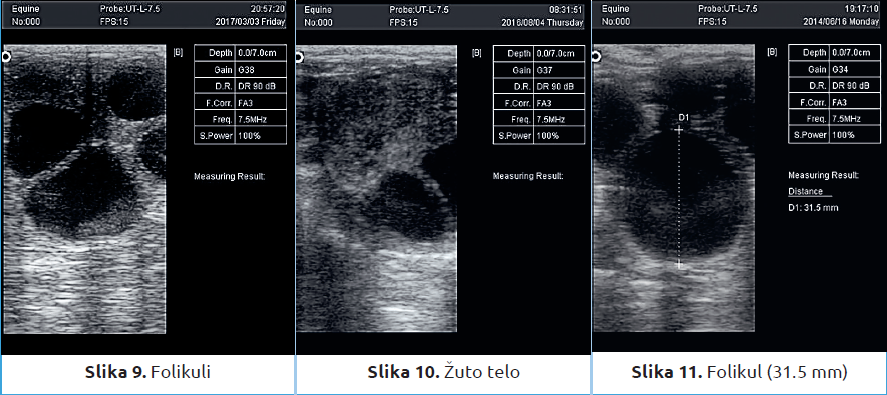
Ultrazvučni pregled se izvodi nakon rektalnog pregleda. Pregledom utvrđujemo prisustvo edema (slika 6), da li u materici postoji tečnost (slika 7) i isključujemo graviditet. Ako u materici postoje endometrijalne ciste treba evidentirati mesto gde se one nalaze (slika 8). Pregledom jajnika se utvrđuje prisustvo folikula (slika 9) ili žutog tela (slika 10) i meri se veličina folikula (slika 11). Nalazi na materici i jajnicima se menjaju dinamično tokom estralnog ciklusa i treba ih obavezno evidentirati u karton veštačkog osemenjavanja kobila.
Vaginalni pregled se izvodi spekulumom nakon što se perinealna regija opere, dezinfikuje i osuši. Pregledom se utvrđuje integritet vestibulovaginalnog sfinktera, prisustvo tečnosti u vagini (gnoj ili urin) kao i boja, vlažnost vaginalnog zida i cerviksa. Ove nalaze takođe treba zabeležiti.
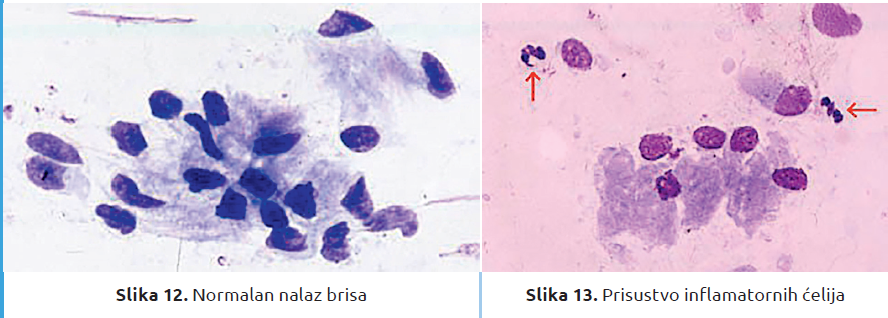
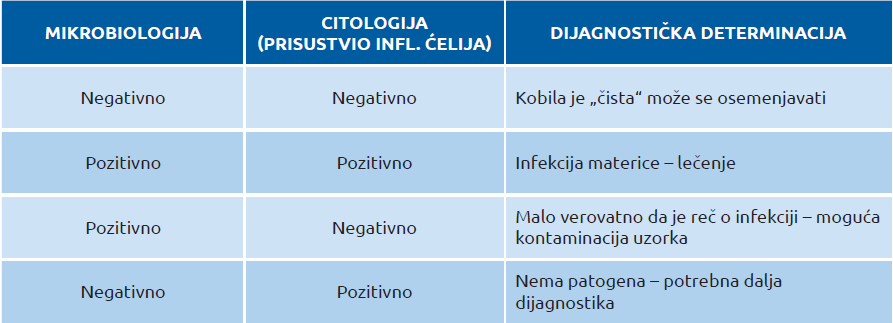
U slučaju da nalaz dobijen rektalnom palpacijom i ultrazvučnim pregledom ukazuje da je materica normalne veličine i konzistencije, da jajnici imaju normalnu aktivnost, a anamnestički podaci ne ukazuju da je kobila ranije pripuštana ili osemenjavana bez uspeha, kobilu možemo osemeniti bez preduzimanja drugih dijagnostičkih procedura. Citološke i mikrobiološke analize treba uraditi kod jalovih kobila, kod oždrebljenih kobila koje su imale povrede vagine i cerviksa u toku porođaja, kod prolapsusa materice ili retencije posteljice. Na raspolaganju nam je i citološka analiza koja se može uraditi u ambulanti, a uzorke možemo poslati na analizu u mikrobiološku laboratoriju. Za uzimanje uzoraka se koriste brisevi koji su posebno pripremljeni za uzorkovanje iz materice. Uzorak koji se nanese na mikroskopsku pločicu oboji se Diff-Quick metodom i posmatra pod mikroskopom (slike 12. i 13). Prisustvo ili odsustvo inflamatornih ćelija, posebno neutrofilnih granulocita ukazuje da li u materici ima znakova inflamacije. Ako oni postoje, treba uraditi i mikrobiološki pregled uzorka. Korišćenjem endometrijalne citologije i mikrobiološkog nalaza, dobijamo mnogo tačniju dijagnozu nego samo mikrobiološkim nalazom. Neki autori smatraju da je odsustvo neutrofilnih granulocita u citološkom nalazu dovoljno da kažemo da je kobila „čista“. Od ostalih dijagnostičkih metoda na raspolaganju su biopsija materice i uteroskopija.
Oprema potrebna za veštačko osemenjavanje kobila zamrznutim semenom
- Kateteri za osemenjavanje kobila (različite dužine, slika 14)
- Stilet za aplikaciju semena
- Vodeno kupatilo za otapanje semena
- Kontejner sa tečnim azotom za čuvanje semena
- Boks (stojnica) (slika 15)
- Mikroskop
- Ultrazvučni aparat sa linearnom endorektalnom sondom (5, 6,5 ili 7,5 MHz).
Protokol veštačkog osemenjavanja kobila zamrznutim semenom
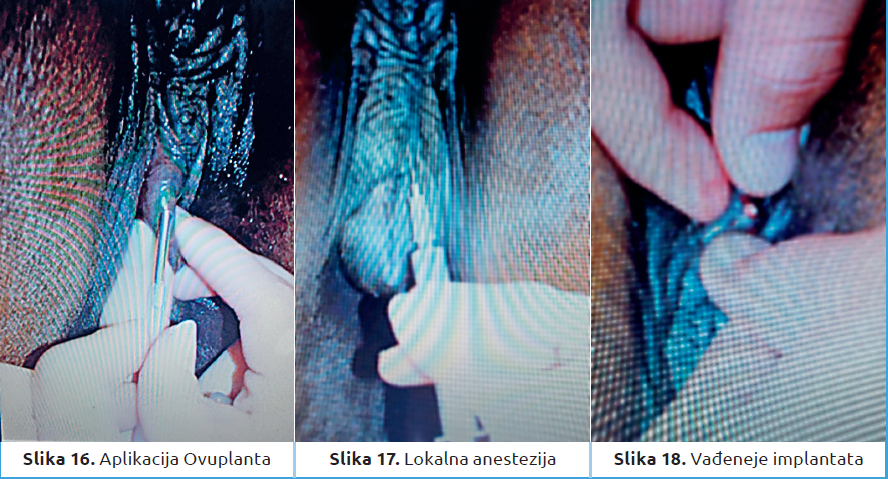
Osemenjavanje kobila zamrznutim semenom zahteva veći broj pregleda od strane veterinara i bilo bi dobro da kobila bude u centru za osemenjavanje (toga u Srbiji nažalost za sada nema), na ergeli na kojoj se kobile osemenjavaju ili na klinici. Kada je prethodnim pregledima utvrđeno da je kobila dobar kandidat za veštačko osemenjavanje zamrznutim semenom, kobila se pregleda ultrazvučnim aparatom svakodnevno ili svaka dva dana dok folikul ne dostigne veličinu od 35 do 40 mm. Ako na jajniku postoji žuto telo, estrus se može indukovati injekcijom Cloprostenola. Kada je folikul veličine 35–40 mm većina kobila ispoljava znake estrusa. Da bi se ubrzala ovulacija tada treba dati hCG ili deslorelin. Češće se upotrebljava hCG, ali neke kobile posle nekoliko aplikacija hCG-a na njega više ne reaguju tako da treba aplikovati GnRH deslorelin (Ovuplant). Preparat se aplikuje u sluznicu vulve (slika 16). Ovaj implantat treba izvaditi nakon ovulacije, da bi se, ukoliko kobila ne ostane ždrebna, sprečio produženi interovulatorni interval ako implantat ostavimo (30 dana) (slike 17 i 18).
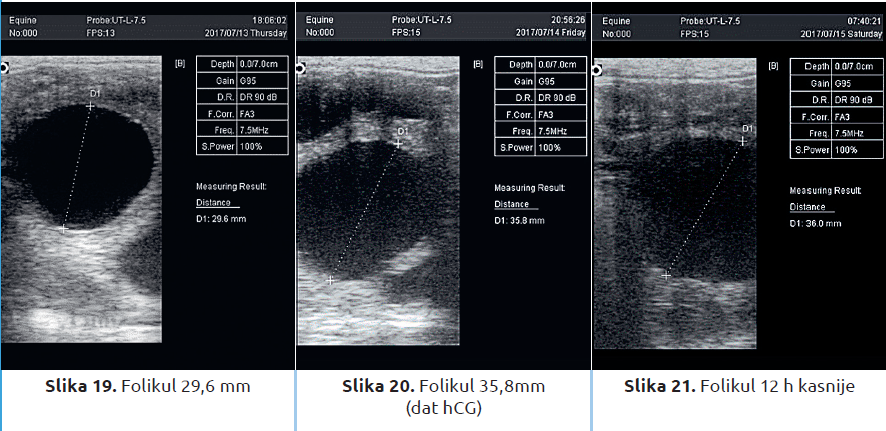
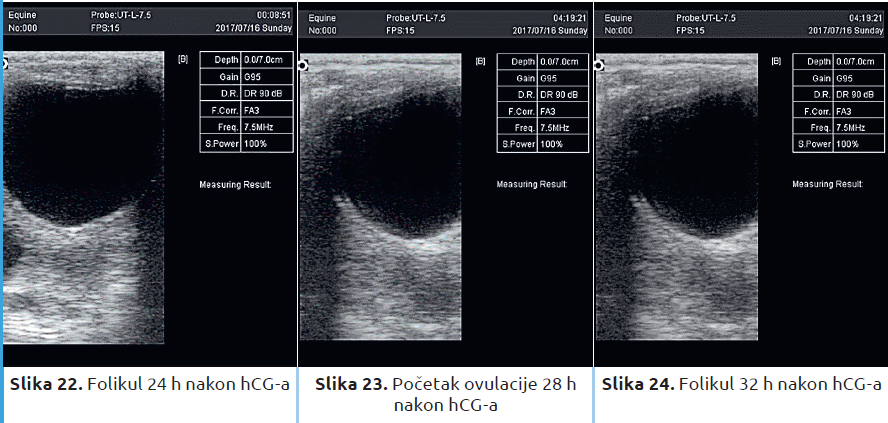
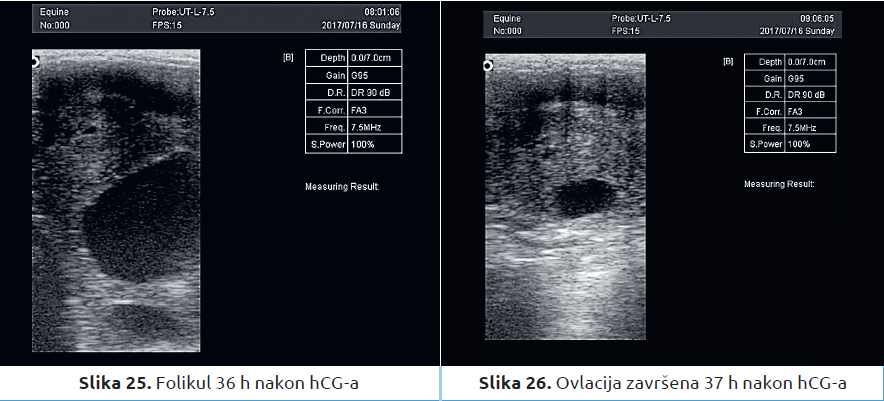
Nakon aplikacije hCG ili GnRH, ovulacija obično nastupi za 36 do 40 časova. Po isteku 24 časa od aplikacije ovih hormona, kobila se pregleda ultrazvučnim aparatom svakih 6 časova dok ne dođe do ovulacije. Nalaze o tonusu materice, eventualnom edemu materice, prisustvu tečnosti, veličini i broju folikula, kao i na kom se jajniku nalazi folikul, potrebno je evidentirati u karton veštačkog osemenjavanja nakon svakog pregleda. Na slikama 19–26 prikazani su rast folikula i ovulacija. Ovde se radi o istom folikulu.
Veštačko osemenjavanje zamrznutim semenom se izvodi od 6 sati pre, do 6 sati nakon ovulacije. Najčešće se kobile osemenjavaju neposredno nakon ovulacije (slika 26. — vreme za VO).
Kobila se uvede u boks, rep se zaštiti, a vulva i perianalni predeo se operu vodom i dezinfikuju povidon jodom, nakon čega se osuše ubrusom. Otapanje semena se vrši u vodenom kupatilu na 37°C u trajanju od 30 s. Obično je seme pakovano u pajetama od 0,5 ml a proizvođač semena daje uputstva o načinu otapanja, kao i koliko pajeta se koristi za jedno osemenjavanje. Najčešće je to 8 pajeta od 0,5 ml, ali može biti 1–2 ili čak i 16 u zavisnosti od pastuva.
Tabela 1. Tumačenje nalaza mikrobiološkog i citološkog pregleda

Veštačko osemenjavanje u rog materice
Veštačko osemenjavanje kobila zamrznutim semenom se može izvoditi kao:
- Standardno osemenjavanje u telo materice
- Osemenjavanje duboko u rog materice (u rog strani jajnika na kome je došlo do ovulacije)
- Osemenjavanje pomoću endoskopa u uterotubalni otvor.
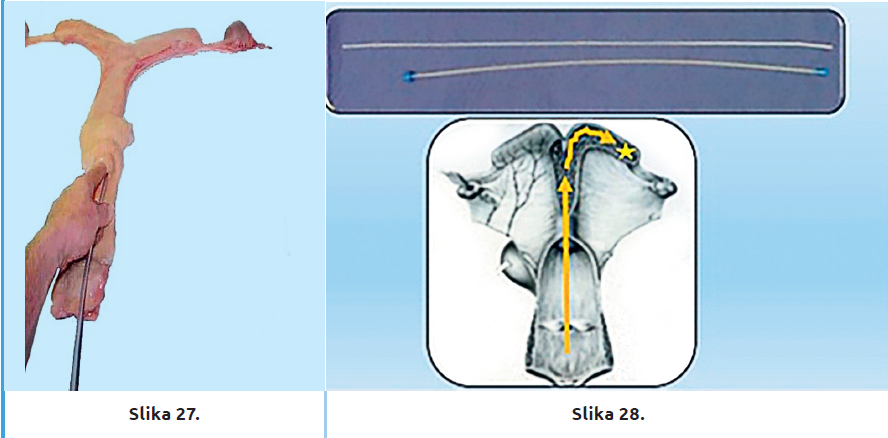
Poslednjih petnaestak godina, kobile se osemenjavaju bimanuelnom metodom duboko u rog na onoj strani gde se nalazi jajnik na kome je ovulirao folikul. Ova tehnika je nešto komplikovanija nego klasično osemenjavanje u telo materice, ali daje mnogo bolje rezultate. Fleksibilni kateter se uvodi rukom vaginalno u cerviks i telo materice, a zatim se rektalno rukom usmerava duboko u rog na onoj strani gde je jajnik na kome je ovulirao folikul (slike 27 i 28). Zatim se pomoću stileta aplikuje određeni broj pajeta. Stilet služi za aplikaciju semena i da se prazna pajeta izvuče iz lumena katetera.
Postoje i drugi protokoli osemenjavanja kobila. Ako ima više doza semena na raspolaganju može se prva doza semena aplikovati 24 sata nakon injekcije hCG ili deslorelina, a druga doza 16 sati kasnije. Takođe se može aplikovati pola doze 24 sata nakon hCG ili deslorelina, a druga polovina se aplikuje 16 sati nakon prve. Ovi protokoli ne zahtevaju toliko česte ultrazvučne preglede.
Pregled kobile nakon veštačkog osemenjavanja
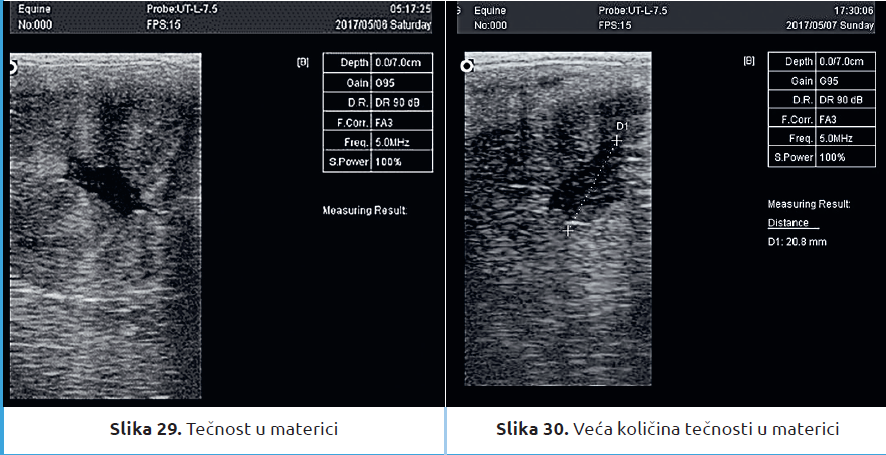
Pregled kobile ultrazvučnom metodom se vrši 18 do 24 časova nakon osemenjavanja. Pri tome se kontroliše prisustvo žutog tela, edema uterusa kao i tečnosti u materici (slike 29 i 30). Retencija intrauterine tečnosti duže od 18 sati nakon osemenjavanja i prisustvo edema materice nakon ovulacije, smanjuju procenat koncepcije. Ovo se najčešće dešava kod starijih kobila (>14 godina) i kod kobila koje imaju lošu perinealnu konformaciju. Radi se endometritisu nastalom nakon osemenjavanja ili pripusta (engl. persistent post-breeding endometritis) i on predstavlja reakciju na egzogeno unet materijal u matericu kao što su komponente semena ili razređivača za seme ili bakterije. To je normalna odbrambena rekcija koja nastaje pola sata nakon osemenjavanja. Manifestuje se pojačanim influksom neutrofilnih granulocita u lumen uterusa gde dolazi do opsonizacije i fagocitoze oštećenih spermatozoida, viška spermatozoida i bakterija. Tom prilikom se oslobađaju prostaglandini koji dovode do kontrakcija materice. Ova odbrambena reakcija uterusa dostiže svoj največi intenzitet (pik) 6 do 12 sati posle inseminacije. Kod reproduktivno zdravih kobila, najveći deo ovih inflamatornih produkata se izbaci normalnim mehanizmima za oko 48 časova nakon inseminacije.
Kod kobila koje imaju usporeni uterini klirens, tečnost se zadržava i nakon ovog vremena. Razlozi za to su: smanjenje frekvence, intenziteta i dužine miometrijalne aktivnosti, vaskularne promene u endometrijumu ili poremećena produkcija mukusa. Takođe, do ovoga mogu dovesti i poremećaji u limfnoj drenaži, kaudo-ventralno pomeranje materice kod starijih kobila koje su se više puta ždrebile kao i parcijalne dilatacije uterusa. Sva ova stanja dovode do inflamacije i akumulacije tečnosti u materici. Priprema zamrznutog semena podrazumeva redukovanje količine seminalne plazme (usled razređenja), a njene komponente su modulatori semenom indukovane inflamacije i štite spermatozoide od opsonizacije i fagocitoze. Neki autori smatraju da je baš ovo razlog što se se kod korišćenja zamrznutog semena javlja izraženija inflamatorna reakcija.
Neophodnost tretmana zavisi od količine tečnosti u materici. Generalno, ako je ona veća od 20 mm u dijametru dovoljna je jedna doza oksitocina (10–20 IU, im). Ako je akumulacija fluida u materici veća od toga, mora se uraditi lavaža uterusa sa 2 l sterilnog zagrejanog fiziološkog rastvora. Nakon toga se nekoliko puta daje oksitocin.
Kod jakog edema materice može se dati neki kortikosteroid, a edem bi trebalo da se povuče nakon ovulacije. Aplikacija kortikosteroida kod jako izraženog edema pre osemenjavanja može da smanji i inflamatornu reakciju.
Dijagnostika graviditeta nakon osemenjavanja
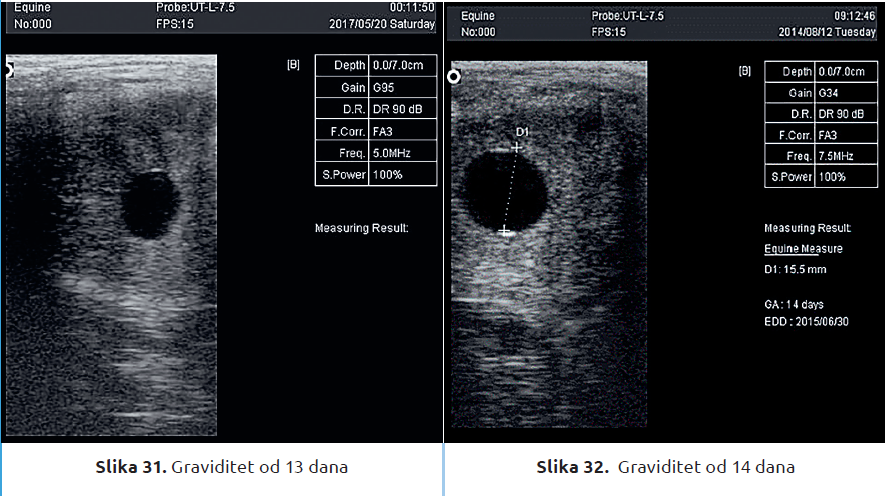
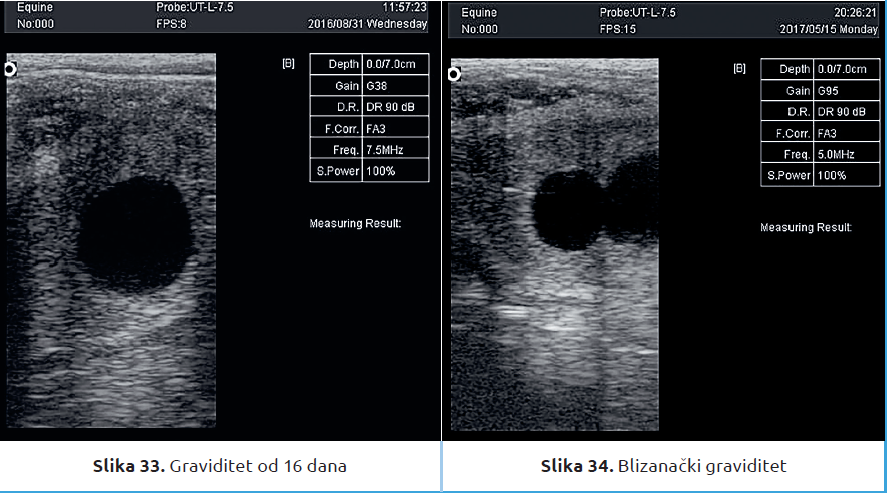
Rana dijagnostika graviditeta se vrši na 14 do 18 dana nakon ovulacije (slike 31, 32, 33). Veoma je važno da se isključi blizanački graviditet (slika 34).
Rezultati uspešnosti osemenjavanja zamrznutim semenom se kreću od 30 do 70 procenata.
Vlasnike kobila svakako treba upoznati sa procedurom kao i rezultatima koji se očekuju, imajući u vidu da je seme pastuva skupo.
Napomena: Sve slike osim 27. i 28. su orginali autora.
Literatura:
1. Guvenc K, ReilasT, Katia T, 2005, Effect of insemination dose and site on uterine inflammatory response of mares, Theriogenology, 63, 9, 2504–12.
2. Hemberg E, Lundeheim N, Einarsson S, 2006, Successful timing of ovulation using deslorelin (Ovuplant) is labor-saving in mares aimed for single ai with frozen semen, Reprod Domest Anim, 41, 6, 535–7.
3. Hunter B, Chirino-Trejo M, Card C, 2006, Uterine inflammatory response to simultaneous treatment with frozen semen and bacteria in resistant mares, AAEP Proceedings, 52, 389–92.
4. Kilicarslan MR, Horoz H, Senunver A, 1996, Effect of GnRH and hCG on ovulation and pregnancy in mares, Vet Rec, 139, 119–20.
5. Kotilainen T, Huhtinen M, Katila M, 1994, Sperm-induced leukocytosis in the equine uterus, Theriogenology, 41, 629–36.
6. Kowalczyk A, Ceniawska-Piatkowska E, Kuczaj M, 2019, Factors Influencing the Popularity of Artificial Insemination of Mares in Europe, Animals, 9, 7, 460.
7. LeBlanc MM, 2009, Infertility in the aged mare, In: N. Edward Robinson, Kim A. Sprayberry, Curent therapy in equine medicine, Sounders Elsevier, Chapter 178, 815–23.
8. Samper CJ, 2009, Newer techniques for artificia insemination, In: N. Edward Robinson, Kim A. Sprayberry, Curent therapy in equine medicine, Sounders Elsevier, Chapter 174, 799–801.
9. Schmidt AR, 2011, How to Breed Mares With Frozen Semen by Deep Horn Insemination, 57, AAEP Proceedings, 48–51.
10. Semper JC, 2001, Management and fertility of mares bred with frozen semen, Anim Reprod Sci, 68, 3–4, 219–29.
11. Sieme H, Bonk A, Hamann H, Klug E, Katia T, 2004, Effects of different artificial insemination techniques and sperm doses on fertility of normal mares and mares with abnormal reproductive history, Theriogenology, 1, 62, 5, 915–28.
12. Sieme H, Bonk A, Ratjen J, Klug E, Rath D, 2003, Effect of sperm number and site/technique of insemination on pregnancy in mares, Pferdeheilkunde, 19, 6, 677–83.
13. Sieme H, Schafer T, Stout TA, Klug E, Waberski D, 2003, The effects of different insemination regimes on fertility in mares, Theriogenology, 1, 60, 6, 1153–64.
14. Troedsson MHT, 1999, Uterine clearance and resistance to persistent endometritis in the mare, Theriogenology, 52, 461–47.
15. Troedsson MHT, Alghamdi AS, Matttisen J, 2002, Equine seminal plasma protects the fertility of spermatozoa in inflamed uterine environment, Theriogenology, 58, 453–6.
16. Troedsson MHT, Loset K, Alghamdi AM, Dahmus B, Crabo BG, 2001, Interaction between equine semen and the endometrium: the inflammatory response to semen, Animal Reproduction Science, 23, 11, 493–6.