 Udruženje vetrinara praktičara Srbije - UVPS
Udruženje vetrinara praktičara Srbije - UVPS
Uzorkovanje na farmama svinja
Autori:
Siniša Milić - Veterinarski specijalistički institut „Sombor“, Sombor (Adresa autora za korespodenciju: sinmilic@gmail.com);
Bratislav Kisin - Veterinarski specijalistički institut „Sombor“, Sombor;
Miroslav Dabić - Veterinarski specijalistički institut „Sombor“, Sombor;
Mira Živadinović - Veterinarski specijalistički institut „Sombor“, Sombor;
Aleksandra Zidarević - Veterinarski specijalistički institut „Sombor“, Sombor;
Vladimir Prokić - Veterinarski specijalistički institut „Sombor“, Sombor;
Zdravko Tomić - Boehringer Ingelheim Serbia d.o.o., Beograd
Kratak sadržaj: Veterinar na farmi svinja ima veliku odgovornost u postavljanju dijagnoze bolesti, a time i donošenju odluka u menadžmentu zdravlja svinja. Veterinarska dijagnostička laboratorija ima važnu ulogu u ovom procesu kroz konsultantske usluge, laboratorijsko testiranje, obradu i distribuciju podataka. Tačnost laboratorijskih rezultata i njihov efekat u rešavanju zdravstvenih problema u velikoj meri zavise od kliničke procene slučaja od strane veterinara na farmi, zatim odabira, kolekcije, pakovanja, obeležavanja, čuvanja i transporta uzoraka. Proces uzorkovanja može biti rutinski, ali često zahteva komunikaciju i planiranje na relaciji laboratorija–veterinar, a u zavisnosti od kompleksnosti problema i dostupnosti testova.
U ovom radu biće prikazane tradicionalne metode uzorkovanja na farmama svinja, kao i modernije, neinvazivne tehnike uzorkovanja.
Ključne reči: dijagnostika, laboratorija, svinje, uzorkovanje
Stalni rast i modernizacija svinjarske proizvodnje omogućavaju lakšu transmisiju patogena, koja predstavlja sve veći izazov za dalju prevenciju, kontrolu i eliminaciju. Analiza panzootije Afričke kuge svinja, jasno ukazuje na činjenicu da su kliničke opservacije previše spore i neprecizne da bi bile baza za efikasne odluke u kontroli ove bolesti. Potrebna je brza, tačna i moderna laboratorijska dijagnostika, kao i adaptacija postojećih metoda ispitivanja na lako dostupne i neinvazivne uzorke.
Odabir uzoraka
Pravilan odabir uzoraka je prva i veoma važna faza od koje zavisi integritet procesa dijagnostike. Radi optimizacije dijagnostičkog ispitivanja, a pre odabira uzoraka, najpre je potrebno razmotriti koja su očekivanja od dijagnostike (uzrok uginuća individualne jedinke, uzrok pojave kliničkih simptoma u grupi životinja i slično), kao i „Šta će biti urađeno sa rezultatima ispitivanja?“. Treće pitanje, koje se odnosi na dizajn protokola uzorkovanja, su troškovi ispitivanja. Radi optimizacije troškova, često se laboratoriji postavlja pitanje o mogućnosti testiranja uzoraka u pulu, ali prilikom odgovora na ovo pitanje treba pažljivo razmotriti senzitivnost dijagnostičkog testa na individualnom nivou, kao i na nivou zapata, odnosno mogućnost dobijanja lažno negativnih rezultata. Pravilan budžet treba da obezbedi tačnu dijagnozu i da omogući da se što preciznije utvrdi zdravstveni status jedinke ili zapata. Kada se jasno definišu očekivanja od laboratorijske dijagnostike, može se pristupiti odabiru uzoraka.
Ukoliko uzorci uzeti u određenoj fazi oboljenja nisu relevantni za odabrani test ili ukoliko se ne odaberu adekvatni uzorci za bolest od interesa, dobiće se lažno negativan rezultat. Odabir uzoraka zavisi od dostupnosti testova, dinamike kretanja bolesti i biologije etiološkog agensa. Kako bi optimizovali vrstu i broj uzoraka potrebno je razmotriti stadijum infekcije (šema 1) kod pojedinačne jedinke ili u populaciji svinja. Na primer, ako je cilj dijagnostike izolacija virusa ili bakterija, uzorkovanje će se izvršiti u latentnom periodu infekcije, kada je infektivni agens prisutan. Sa druge strane, ukoliko je cilj da detektujemo antitela protiv specifičnog agensa, uzorkovanje mora da se izvrši nakon određenog vremena, koje je potrebno da se razviju antitela do nivoa kada se mogu detektovati, a tada često nije moguće utvrditi prisustvo uzročnog agensa. Ova dinamika je varijabilna i zavisi od uzročnog agensa i odabira specifičnog serološkog testa.
U populacijama svinja, bolest je često prisutna u kontinuitetu, što nam omogućava detekciju pojedinačnih slučajeva u različitim fazama bolesti i primenu različitih tehnika uzorkovanja. Odabir jedinki sa simptomima akutne bolesti povećava šansu da se detektuje uzročni agens, njegovi antigeni ili genom. Pri odabiru uzoraka veoma je bitno poznavanje biologije uzročnog agensa (lokalizacija u organizmu, otpornost na spoljašnje uticaje i slično). Poznavanje biologije uzročnog agensa je bitno i zbog činjenice da se pojedine bakterije (E. coli) nalaze i u crevnom sadržaju zdravih svinja. U tim slučajevima, njihov nalaz nema klinički značaj, ali ako se uzorci uzmaju od svinja sa kliničkim i morfološkim simptomima digestivne bolesti i potom se izolati tipiziraju, rezultati često mogu ukazati na značaj uzročnika u nastanku oboljenja.
Veterinar na farmi najviše vremena treba da provede na opservaciji svinja, praćenju znakova poremećaja opšteg zdravstvenog stanja i tek kad ima kompletne podatke o istoriji bolesti može da pristupi odabiru svinja od kojih će se uzeti uzorci, bilo da je reč o uzorcima krvnog seruma, briseva, oralne tečnosti ili odabiru svinja za obdukciju.
Uzimanje uzoraka sa obdukcije
Obdukcija uginulih svinja je od velike važnosti za veterinare na farmi zbog toga što im obezbeđuje potpunije razumevanje i praćenje procesa bolesti, edukaciju, kao i ranu detekciju novih pretnji po zdravlje životinja. „Oči i ruke“ patologa su najbolji početak kvalitetnog istraživanja uzroka uginuća. Nedavno uginule ili na human način eutanazirane životinje, koje su prethodno imale simptome akutne bolesti, uvek imaju prioritet prilikom odabira životinja za obdukciju. Obdukcija predstavlja plansko otvaranje i sistematski pregled leša s ciljem utvrđivanja, proučavanja i objašnjenja patološko-anatomskih promena na osnovu kojih treba doneti zaključak o uzroku smrti ili postojanju bolesti.
Sa obdukcije se prevashodno uzorkuju delovi makroskopski promenjenih organa i korespodentni limfni čvorovi, ali je preporučljivo uzorkovati i druge organe. U nekim slučajevima, za dijagnostiku i uzorkovanje je dovoljan samo jedan organ, kao što su pluća i traheobronhijalni limfni čvorovi kod respiratornih bolesti. Ukoliko obdukciju izvodi veterinar na farmi, neophodno je da podatke sa obdukcije detaljno unese u propratni akt, koji prati uzorke. Prilikom uzimanja uzoraka sa obdukcije, potrebno je voditi računa da se spreči unakrsna kontaminacija, tako što se za uzorkovanje od svake naredne jedinke uzimaju čiste rukavice i pribor, a creva i sadržaj creva se otvaraju i uzorkuju na kraju. Uzorci uzeti sa obdukcije moraju biti jasno obeleženi i upakovani u nepropusnu ambalažu, a za mikrobiološku analizu i sterilnu ambalažu i transportuju se do laboratorije u hladnom lancu, na temperaturi frižidera.
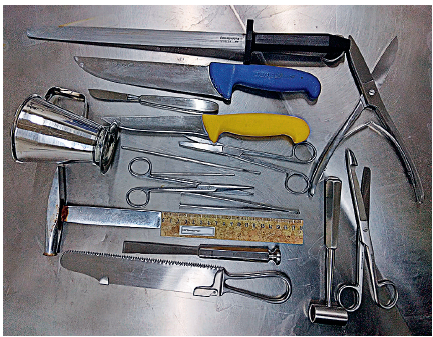
Slika 1. Oprema za obdukciju.
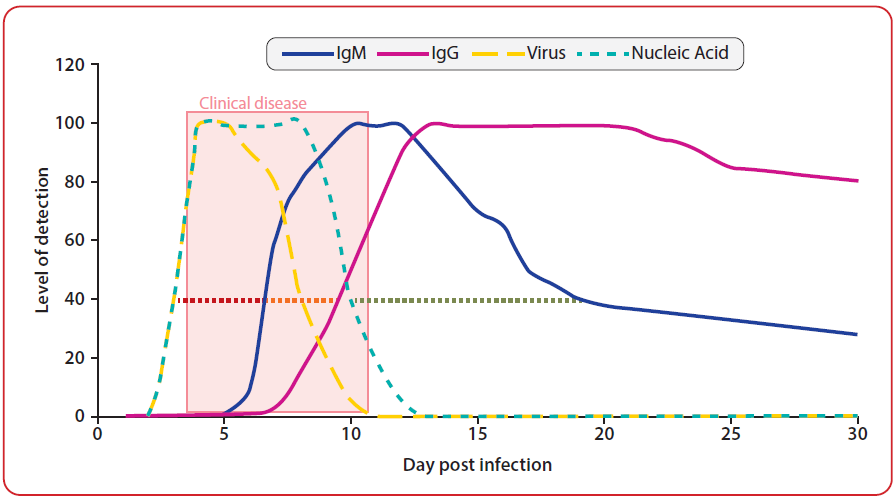
Slika 1. Stadijum infekcije
(preuzeto sa: https://rr-asia.oie.int/wp-content/uploads/2020/06/2_swine-disease-diagnosis_morrisy-qa.pdf).
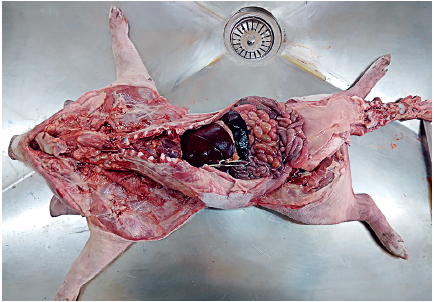
Slika 2. Otvorena grudna i trbušna šupljina praseta.
Uzorkovanje materijala za histopatološka i imunohistohemijska ispitivanja
Histopatološka analiza daje korisne informacije o mikroskopskim promenama kod suspektne bolesti, ali ne retko, može da sugeriše i na alternativne promene, koje nisu vidljive okom, a koje su od značaja za razumevanje patološkog procesa. Sve više je u primeni i imunohistohemijsko ispitivanje, koje omogućava vizuelizaciju antigena (npr. uzročnog agensa) i njegovu distribuciju u tkivima.
Uzorci za histopatološka i imunohistohemijska ispitivanja se uzimaju što pre je moguće, najbolje odmah po uginuću životinje. Pravilo je da se uzimaju delovi makroskopski promenjenih organa, ali i onih koji nisu promenjeni, kao što su uzorci srca, pluća, jetre, slezine, bubrega, creva i mozga. Kod ograničenih promena, uzorak se uzima na granici promenjeng i zdravog dela, dok se kod raširenih promena uzima više uzoraka. Dimenzije tkivnog isečka treba da budu 1 × 1 × 0,5 cm i on se potapa u najmanje 10 puta veću količinu 10% neutralnog formalina. Uzorkovano tkivo se unosi u posude sa širokim poklopcem sa zavrtnjem, da bi se sprečilo prosipanje i isparavanje formalina. Posude se jasno obeležavaju vodootpornim flomasterom i uz popunjen propratni akt šalju do laboratorije na sobnoj temperaturi.
Uzorkovanje materijala za mikrobiološka ispitivanja
Izbor jedinki, selekcija i transport uzoraka si najkritičniji momenti od kojih zavisi celokupan tok i ishod mikrobiološke dijagnostike. Ukoliko se ovde, na samom početku, ne poštuju određeni mikrobiološki principi, rezultati ispitivanja će vrlo verovatno biti potpuno irelevantni za postavljanje dijagnoze. Zbog toga je komunikacija između mikrobiologa i laboratorijskog osoblja sa jedne strane, kao i osobe koja vrši uzorkovanje sa druge strane, izuzetno važna i neophodna. Ovo je posebno važno u slučaju potrebe identifikacije određenih kulturelno zahtevnih mikroorganizama, gde će se osim rutinskih primeniti i posebne vrste mikrobioloških podloga.
Osnovne smernice za uzorkovanje materijala za mikrobiološka ispitivanja su sledeće: Uzorci koji se šalju u laboratoriju treba da potiču od živih ili nedavno uginulih jedinki. Ukoliko su životinje žive, najbolje je da se šalju uzorci od akutno obolelih jedinki, sa tipičnim simptomima bolesti. Uzorci treba da se uzmu sa zahvaćenog područja što je ranije moguće, nakon pojave kliničkih simptoma. Ovo je naročito važno za virusne infekcije jer se smatra da je koncentracija virusa maksimalna u ranim fazama infekcije. Ukoliko je moguće, uzorci se uzimaju posebno od eutanaziranih ili kontaktnih životinja zbog toga što su one najčešće u ranoj fazi infekcije. Prilikom uzorkovanja, biraju se rubni delovi promenjenih tkiva tako da uzorak uvek sadrži i deo tkiva koji makroskopski nije promenjen. Replikacija mikroorganizama je najveća na obodu lezije. Izuzetno je važno uzorke uzimati aseptično, koliko god je to moguće u terenskim uslovima. Ciljne mikroorganizme vrlo lako preraste kontaminirajuća mikroflora čime se dobijaju lažno negativni i/ili neodgovarajući rezultati laboratorijskog ispitivanja. Uzorci se uvek uzimaju pre aplikacije bilo kakvih lekova. Uzorci za mikrobiološka ispitivanja koji potiču od životinja nedavno tretiranih antibioticima imaju veoma mali značaj u izolaciji bakterija.
Materijal koji se šalje na suvim brisevima je podložan isušivanju čime se tokom perioda transporta eliminišu mikroorganizmi osetljivi na desikaciju (na primer rod Streptococcus). Takođe, ni sama količina uzorka na brisu nije dovoljna naročito ako je potrebno inokulisati više različitih podloga. Zbog toga, brisevi ne predstavljaju idealan način uzorkovanja za mikrobiološka ispitivanja te ih treba izbegavati. Izuzetak predstavljaju komercijalno dostupni brisevi sa transportnom podlogom (slika 3), pomoću kojih se održava vijabilnost uzročnika. Kad god je to moguće, uzorak za mikrobiološka ispitivanja treba da sadrži komad tkiva veličine oko 2–5 cm (min. 4 cm3). Organi grudne šupljine, parenhimatozni organi trbušne šupljine kao i creva i njihov sadržaj se obavezno uzorkuju, pakuju i obeležavaju odvojeno (slika 4). Tečni uzorci (mleko, urin, punktat) pakuju se u sterilne posude (slika 5) u zapremini od oko 2–5 ml. Ukoliko se uzorkuju gnojne promene, pored samog gnojnog sadržaja mora se uzorkovati i kapsula apscesa zbog toga što sam gnoj gotovo nikad ne sadrži vijabilne mikroorganizme.
Vrsta i poreklo uzorka moraju biti adekvatni sa apekta vrste ispitivanja i vrste mikroorganizma čija se izolacija očekuje. Tako, na primer, bakterija Haemophylus parasuis brzo propada na višim temperaturama, pa je veoma bitno da se uzorkovanje kod suspektnih slučajeva izvrši neposredno po uginuću životinje i da se uzorci u što kraćem roku i u hladnom lancu transportuju do dijagnostičke laboratorije. Drugi aspekt je lokalizacija na kojoj infektivni agens ispoljava svoje patogeno dejstvo. Dobar primer je bakterija Brachyspira hyodysenteriae koja se lokalizuje u debelim crevima, pa je uzorak izbora za dijagnostiku ove bakterije debelo crevo ili feces. Ukoliko se uzorkuju delovi tankih creva, ovaj agens neće biti otkriven. U slučaju bilo kakvih nedoumica u vezi sa ovim, najbolje je odmah kontaktirati laboratoriju.
Ako životinje ispoljavaju tipične simptome respiratornih oboljenja, sa aspekta mikrobiologije je izuzetno važno da li će se u laboratoriju poslati bris nosne/ždrelne šupljine, respiratornih puteva ili lezije na plućima. Broj i vrsta potencijalnih patogena se ekstremno razlikuju u zavisnosti od mesta uzorkovanja. Ukoliko se prilikom uzorkovanja posumnja na neki određeni mikroorgarnizam to mora da se navede u propratnom aktu, kako bi laboratorija mogla da primeni odgovarajući metod kultivacije (na primer anaeroban rast klostridija ili specijalne podloge za rast Actinobacillus i Haemophylus vrsta).
Tkiva, telesne tečnosti i brisevi namenjeni mikrobiološkom ispitivanju treba da se transportuju u hladnom lancu, na temperaturi frižidera i da se dostave u laboratoriju što pre, a najkasnije 24 sata od momenta uzorkovanja.
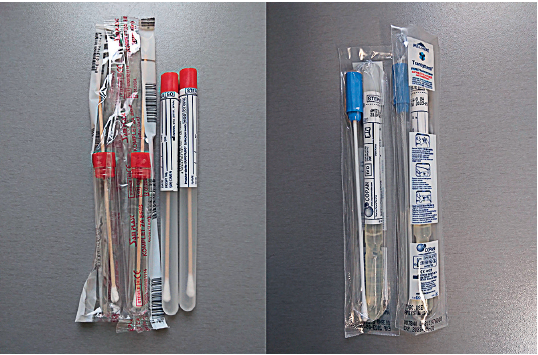
Slika 3. Brisevi za uzorkovanje.
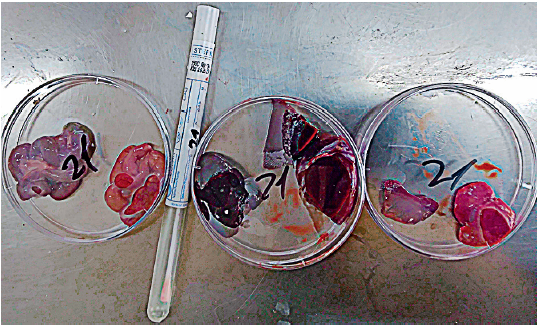
Slika 4. Uzorci za mikrobiološka ispitivanja.

Slika 5. Posude za uzorkovanje.

Slika 6. Sterilna kesa za uzorkovanje.
Uzorkovanje materijala za molekularna ispitivanja
Razvoj molekularnih metoda (PCR, real time PCR) je revolucionaran u različitim oblastima medicine, pa i u oblasti mikrobiologije. Ova tehnologija se konstantno unapređuje i razvijaju se jeftinija i efikasnija rešenja (simultana detekcija više patogena — multipleks PCR i slično). Primena ove tehnologije doprinosi mnogo efikasnijoj kontroli bolesti, održivoj proizvodnji i unapređenju dobrobiti životinja.
Molekularne metode ispitivanja imaju nekoliko značajnih prednosti u odnosu na klasične metode mikrobiološke dijagnostike. Neke od prednosti ove tehnologije su brzina dobijanja rezultata, specifičnost, detekcija patogena koji se teško kultivišu, manje rizična detekcija opasnih patogena, olakšana i preciznija tipizacija mikroorganizama. Pored toga, integritet nukleinskih kiselina je mnogo bolje očuvan tokom određenog vremenskog perioda nego vijabilnost tih istih mikroorganizama, zatim nukleinske kiseline mikroorganizama perzistiraju u organizmu životinje i nakon inicijalnog tretmana čime je njihovo dokazivanje omogućeno iako kulturelno više nije. Na kraju, molekularne metode odlikuje visoka osetljivost, što znači da mogu da se izvedu sa znatno manjom količinom uzorka i uz primenu manje invazivnih tehnika uzorkovanja. Upravo visoka senzitivnost predstavlja jedan od glavnih problema prilikom uzimanja uzoraka za ovu vrstu ispitivanja. Naime, molekularnim metodama moguće je dokazati prisustvo tek nekoliko ciljnih DNK/RNK fragmenata (manje od 10), što znači da se posebno mora voditi računa o kontaminaciji (strogo menjanje rukavica i pribora za uzorkovanje, pakovanje u nepropusnu ambalažu koja može da se zatvori i sl.).
Kao uzorci za molekularna ispitivanja mogu da posluže različite vrste briseva, koža, tkiva, kosti, krv, semena tečnost, mleko, plјuvačka, feces ili bilo koji drugi materijal koji sadrži nukleinske kiseline. Najčešći uzorci za detekciju većine uzročnika zaraznih bolesti svinja su krv, tkiva i brisevi. Za PCR analize se uzorkuje oko 2 ml krvi u vakutajnere sa dodatkom EDTA (ljubičasti čep; slika 7). Za uzorkovanje tkiva i telesnih tečnosti mogu se koristiti i kartice sa filter papirom (FTATM Classic Card, Insta DNATM Cards; slika 8), koje su specijalno dizajnirane za čuvanje i transport uzoraka za molekularna ispitivanja. Uzorci koji će se testirati u pulu, treba da se uzorkuju individualno i da se jasno obeleže. Uzorci za molekularna ispitivanja se pakuju u plastične kese ili posude koje mogu čvrsto da se zatvore i na temperaturi frižidera se transportuju do laboratorije.
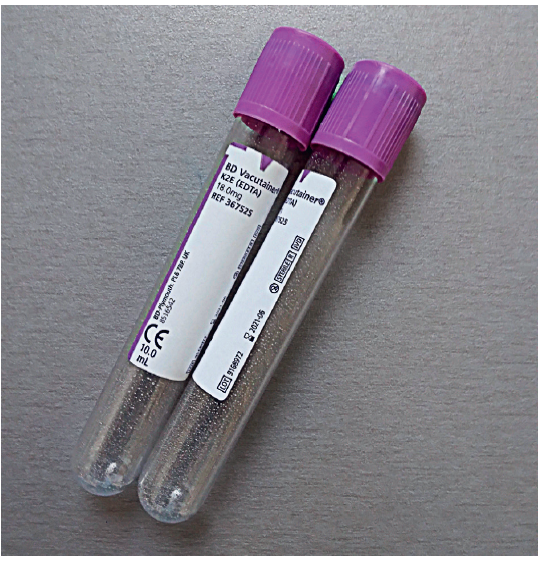
Slika 7. Vakutajner za uzorkovanje pune krvi sa EDTA antikoagulansom.

Slika 8. Oprema koja se koristi za uzorkovanje materijala za molekularna ispitivanja.
Uzorkovanje materijala za parazitološka ispitivanja
Razvojni stadijumi većine parazita mogu biti detektovani u fecesu, krvi, sputumu ili skarifikatu kože. Za parazitološka ispitivanja na farmama svinja, najčešće se uzimaju uzorci fecesa. Feces se uzorkuje direktno iz creva prilikom obdukcije ili kolekcijom uzoraka iz okoline i pakuje se u plastične posude sa poklopcem ili kese sa zatvaračem u količini od oko 10 g. Nekada se šalju delovi organa ili celi organi sa promenama suspektnim na parazitsku infekciju. Vidljivi ektoparaziti ili nematode mogu da se transportuju do laboratorije potopljeni u 70% alkohol. Uzorci za parazitološka ispitivanja se jasno obeleže i transportuju se u hladnom lancu na temperaturi frižidera.
Uzorkovanje za serološka ispitivanja
Serološka ispitivanja se koriste za detekciju određenih klasa antitela u serumu, najčešće IgG. Antitela se stvaraju nakon određenog perioda vremena posle infekcije ili vakcinacije (aktivni imunitet) ili se sa kolostrumom dobijaju od majke (pasivni imunitet). Serološkim testovima se uglavnom detektuju stare infekcije, zatim postvakcinalna antitela i ustanovljava se prevalenca ili potvrđuje odsustvo bolesti na farmi. Kada se ovi testovi koriste za dijagnostiku bolesti kod pojedinačnih jedinki ili u grupi, često su za adekvatan rad potrebni parni uzorci seruma uzeti u razmaku od 2–3 nedelje. Višestruko povećanje titra antitela u parnom serumu je jasan indikator sveže infekcije. Ukoliko nema značajnog povećanja titra antitela u parnom serumu, a oba seruma su pozitivna, reč je o staroj infekciji/vakcinaciji.
Krv se za serološka ispitivanja kod svinja najčešće uzorkuje punkcijom jugularne vene, prednje šuplje vene ili ušne vene u epruvetu bez dodataka ili sa dodatim aktivatorom koagulacije (crveni čep; slika 9) ili u epruvetu sa gelom za separaciju seruma (žuti čep). Uzorak zatim treba držati na sobnoj temperaturi u trajanju od 30–60 minuta da bi se omogućilo formiranje ugruška i odvajanje seruma, a zatim se čuva i transportuje u hladnom lancu na temperaturi frižidera. Eritrociti svinja su veoma osetljivi na hemolizu.
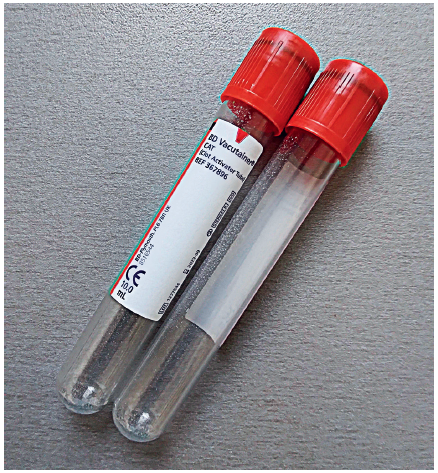
Slika 9. Vakutejner za uzorkovanje krvnog seruma.
Grubo rukovanje sa uzorkom, smrzavanje i pregrevanje uzorka ili nepotpuno odvajanje eritrocita od seruma može dovesti do hemolize, koja u zavisnosti od stepena, može imati negativan uticaj na rezultate pojedinih seroloških testova.
Moderne tehnike uzorkovanja
Tradicionalne metode dijagnostike bolesti na farmi zahtevaju uzorkovanje krvi ili različitih tkiva, što je stresno za životinje i zahteva određene veštine, vreme i troškove. Modernije metode uzorkovanja, kao što su uzorkovanje oralne tečnosti i procesne tečnosti, omogućavaju detekciju nekoliko važnih bolesti, bilo na individualnom nivou ili na nivou zapata. Obe metode uzorkovanja su pogodne za detekciju bolesti u ranoj fazi, zahtevaju relativno malo vremena i nisu ili su minimalno stresne za životinje.
Oralna tečnost je mešavina pljuvačke i transudata oralne sluznice, a dobija se ceđenjem pamučne užadi, koje su svinje prethodno žvakale (slika 11). Oralna tečnost se uzorkuje od svinja starijih od 21 dana. Uže se postavlja tako što se veže za ogradu boksa, u visini ramena svinja i to najbolje rano ujutro nakon buđenja, a pre hranjenja. Kada se prvi put uzorkuje, obično je potrebno i do 60 minuta, a kasnije se svinje brzo naviknu i uzorkovanje traje 20–30 minuta. Rezultati istraživanja ukazuju da uzorak oralne tečnosti dobijen iz jednog užeta, postavljenog u boks u kom se nalazi oko 25 svinja, u trajanju od 30 minuta, reprezentuje status od oko 80 procenata životinja smeštenih u taj boks. Uže se može odmah iscediti u bocu sa poklopcem ili se pakuje u nepropusnu PVC kesu, jasno obeleži i u hladnom lancu transportuje do dijagnostičke laboratorije.
Iz oralne tečnosti mogu se detektovati antitela protiv: Afričke kuge svinja (AKS), klasične kuge svinja (KKS), reproduktivno respiratornog sindroma svinja (PRRS), cirkovirusa svinja tipa 2 (PCV2), virusa influence tipa A i nekih drugih uzročnika. Pored toga, iz oralne tečnosti se mogu detektovati i specifični delovi genoma: AKS, KKS, PRRS, PCV2, virusa influence tipa A, virusa Aujeckijeve bolesti svinja, cirkovirusa svinja tipa 3 (PCV3), virusa epidemične dijareje svinja (PEDV), virusa transmisivnog gastroenteritisa svinja (TGEV), delta korona virusa svinja (PDCoV), parvovirusa svinja (PPV), rotavirusa svinja, Mycoplasma hyopneumoniae i drugih. Lista uzročnika oboljenja, čija je detekcija iz oralne tečnosti svinja potvrđena se stalno proširuje.
Umesto da se odbace, testisi i repovi dobijeni kastracijom i sečenjem repova prasadi se pakuju u nepropusne plastične kese, koje se obeležavaju i u hladnom lancu transportuju do laboratorije. U laboratoriji se iz ovih uzoraka filtracijom dobija procesna tečnost. Uobičajeno je da jedan uzorak predstavljaju testisi i repovi od 5–6 legala prasadi. Ovaj uzorak je veoma dragocen jer nam omogućava detekciju bolesti u ranoj fazi u prasilištu (slika 12). Iz procesne tečnosti, primenom molekularnih metoda, mogu se detektovati specifični delovi genoma PRRS, PCV2, PCV3, PEDV, Mycoplasma hyopneumoniae i drugih.

Slika 10. Oprema za uzorkovanje oralne tečnosti
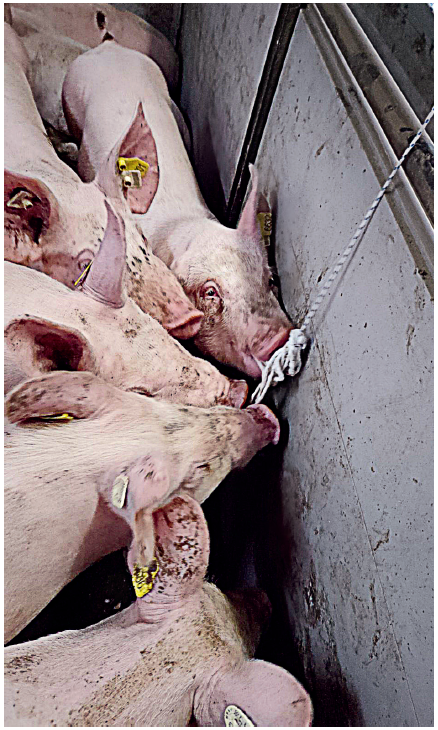
Slika 11. Uzorkovanje oralne tečnosti
Obeležavanje i pakovanje uzoraka
Svaka laboratorija treba da ima definisan propratni akt, koji je potrebno što detaljnije popuniti, a koji sadrži podatke o naručiocu ispitivanja, vlasniku, vrsti, rasi, polu, starosti, obeležju životinje, kliničkim siptomima, makroskopskim lezijama, prethodnom tretmanu, vakcinaciji, morbiditetu i mortalitetu u grupi životinja, uzetim uzorcima i traženim testovima. Ukoliko je suspektna zoonozna bolest, to mora jasno da se naznači. Propratni akt se pakuje u kesu koja ne propušta vodu i transportuje zajedno sa uzorkom.
Osnovni princip pakovanja uzoraka je da se koristi trostruka ambalaža. Primarna ambalaža može da bude kesa (slika 6), epruveta ili druga plastična posuda (slika 5), koje mogu da se zatvore. Špricevi, rukavice i kese bez mogućnosti zatvaranja nisu pogodna ambalaža za transport. Tečni uzorci se pakuju u posude sa poklopcem. Posude sa uzorcima moraju biti jasno obeležene i za to se koriste vodootporni flomasteri.
Ovako zatvorena i obeležena primarna ambalaža se zatim zatvara u sekundarnu ambalažu (nepropusna kesa) koja sadrži adsorbentni materijal (papirna vata). Sekundarna ambalaža se zatim pakuje u transportni kontejner–tercijarna ambalaža, a obično je to ručni frižider. Ova ambalaža treba da sadrži rashladno sredstvo i materijal koji treba da zaštiti uzorke (stiropor ili slično). Sredstva za rashlađivanje ne treba da budu u direktnom kontaktu sa uzorcima već se pakuju u nepropusne kese.
Kontinuirani rast i razvoj svinjarske proizvodnje, kao i uvođenje sofisticirane tehnologije na farmama svinja predstavljaju sve veći izazov za veterinara na farmi, od koga se očekuje veći nivo znanja i ekspertize. Da bi se odgovorilo na ove izazove i da bi se uspostavila efikasna kontrola zdravstvenog stanja svinja, značajna je uloga veterinarske dijagnostičke laboratorije. Kako bi bili odabrani odgovarajući uzorci i testovi i kako bi rezultati laboratorijskog ispitivanja bili pravilno interpretirani i upotrebljeni, od ključnog značaja je dobra komunikacija između veterinara na farmi i veterinarske dijagnostičke laboratorije.

Slika 12. Uzorci procesne tečnosti

Slika 13. Laboratorija Veterinarskog specijalističkog instituta „Sombor“
Literatura:
1. Aiello Susan E, Moses Michael A, 2016, The Merck Veterinary Manual, eleventh edition, Kenilworth, NJ, Merck & Co, Inc.
2. Almeida et al., 2021, Longitudinal piglet sampling in commercial sow farms highlights the challenge of PRRSV detection, Porcine Health Management.
3. Carter GR, Cole JR, 1990, Diagnostic Procedures in Veterinary Bacteriology and Mycology, fifth edition
4. Gramer M, Rossow K, Torrison J, 2005, A Guide to Porcine Sample Submission and Diagnostic Tests, University of Minnesota Veterinary Diagnostic Laboratory.
5. Henao-Diaz et al., 2020, Guidelines for oral fluid-based surveillance of viral pathogens in swine, Porcine Health Management.
6. Marinković D, Nešić V, 2013, Tehnika obdukcije životinja sa osnovama tanatologije, Fakultet veterinarske medicine Univerziteta u Beogradu.
7. Markey BK, Leonard FC, Archambault M, Cullinane A, Maguire D, 2013, Clinical Veterinary Microbiology, Edinburgh, Elsevier.
8. Milićević V, Kureljušić B, Maksimović Zorić J, Veljović LJ, Jezdimirović N, 2019, Upotreba oralne tečnosti za dijagnostiku zaraznih bolesti svinja na nivou populacije, Zbornik kratkih sadržaja, 21 Simpozijum epizootiologa i epidemiologa, Novi Sad.
9. Murato Y, Hayama Y, Shimizu Y, Sawai K, Yamamoto T, 2020, Evaluation of sampling methods for effective detection of infected pig farms during a disease outbreak, PLoS ONE 15(10): e0241177.
10. Quinn PJ, Carter ME, Markey B, Carter GR, 1993, Clinical Veterinary Microbiology 1st edition, Mosby ltd.
11. Schwartz WL, 1982, Laboratory Diagnosis of Swine Diseases, Vet Clin North Am Large Anim Pract, 201–223.
12. Thompson David, Benjamin Madonna, 2019, Sampling Oral and Processing Fluids to Identify Disease in Pigs, Michigan State University.
13. White D, Rotolo M, Olsen C, Wang C, Prickett J, Kittawornrat A, et al., 2014, Recommendations for pen-based oral-fluid collection in growing pigs, J Swine Heal Prod, 22:138–41.
14. Zimmerman Jeffrey J, Karriker Locke A, Ramirez A, Schwartz Kent J, Stevenson Gregory W, et al., 2012, Diseases of Swine, 10th edition, Willey Blackwell.