 Udruženje vetrinara praktičara Srbije - UVPS
Udruženje vetrinara praktičara Srbije - UVPS
Značaj mikrobioma u savremenoj živinarskoj proizvodnji [2. deo]
Autori:
Milanko Šekler - Veterinarski specijalistički institut „Kraljevo“, Kraljevo, Srbija;
Dejan Vidanović - Veterinarski specijalistički institut „Kraljevo“, Kraljevo, Srbija;
Bojana Tešović - Veterinarski specijalistički institut „Kraljevo“, Kraljevo, Srbija;
Nikola Vasković - Veterinarski specijalistički institut „Kraljevo“, Kraljevo, Srbija;
Marko Dmitrić - Veterinarski specijalistički institut „Kraljevo“, Kraljevo, Srbija;
Kazimir Matović - Veterinarski specijalistički institut „Kraljevo“, Kraljevo, Srbija;
Zoran Debeljak - Veterinarski specijalistički institut „Kraljevo“, Kraljevo, Srbija
Kratak sadržaj: Ove godine, živinsko meso će postati najviše proizvedeno i konzumirano meso na svetu. Očekuje se da će njegova potražnja i dalje rasti, kako bi se zadovoljile potrebe za životinjskim proteinima kod sve veće populacije ljudi. Gastrointestinalni trakt živine je gusto naseljen populacijom mikroorganizama koji blisko i intenzivno stupaju u interakciju sa organizmom domaćina i hranom koja se vari. Mikrobiom creva koristi organizmu domaćina obezbeđujući mu dodatne hranljive sastojke, od inače slabo iskoristivih delova hrane, modulirajući razvoj i funkciju digestivnog trakta i imunskog sistema domaćina. Zauzvrat, organizam domaćina pruža stanište i hranljive materije za rast i razmnožavanje bakterija mikrobioma. Zdravstveni status creva živine ima veliki uticaj na sistemsko zdravlje ptica, dobrobit životinja, efikasnost živinarske proizvodnje, bezbednost hrane i uticaj na životnu sredinu. Skoriji napredak u razvoju tehnologije sekvenciranja (sledeća generacija sekvenciranja), kao metode za identifikaciju i popisivanje svih bakterijskih vrsta prisutnih u nekoj životnoj sredini, probudio je interes za proučavanje uloge mikrobioma creva živine na njihovo zdravlje i produktivnost. Bolje razumevanje funkcije pilećih creva i njihovog mikrobioma pružiće nove mogućnosti za poboljšanje zdravlja živine i živinarske proizvodnje. Značaj ove teme je značajno porastao tokom poslednje dve decenije. Ovaj pregledni rad objedinjuje najnovije informacije o glavnim faktorima koji oblikuju proces sticanja i sazrevanja mikrobioma creva, njihovoj interakciji sa pilećim imunskim sistemom i rezultatima tih interakcija na zdravstveni status creva i produktivnosti jedinki.
Ključne reči: gastrointestinalni trakt, mikrobiološka zajednica creva, mikrobiom, sekvenciranje, živina
Faktori koji utiču i oblikuju intestinalni mikrobiom živine
Shema 1. prikazuje ključne faktore životne sredine i domaćina koji oblikuju intestinalni mikrobiom creva živine i njihovu interakciju sa proizvodnim performansama živine.
Sticanje, razvoj i sazrevanje intestinalnog mikrobioma živine
Inicijalna kolonizacija gastrointestinalnog trakta živine mikroorganizmima počinje da se odigrava prirodim putem od momenta izleganja mada najnovija istraživanja ukazuju da proces kolonizacije može početi čak i pre i to tako što mikroorganizmi prođu kroz pore na ljusci jajeta još pre izlegnuća (Lee S. i sar., 2019, Roto S. M. i sar., 2016).
Intenzivna živinarska proizvodnja implementira veoma striktne i snažne higijenske mere koje drastično smanjuju unošenje mikroorganizama u okruženje gde se izvodi leženje pilića, a sve u cilju da se izbegne rana kolonizacija digestivnog trakta pilića patogenim bakterijama i da tako novoizleženi pilići steknu početni mikrobiom u kontrolisanim uslovima farmi za njihov odgoj umesto prirodnim putem (na inkubatoru ili od kokoške – kvočke) (Donaldson E. E. i sar., 2017). Međutim, neki dostupni radovi podržavaju takođe i hipotezu da deo mikroorganizama kolonizatora, u stadijumu ranog embriona, može biti nasleđen i od kokoške (kvočke) koji se takođe mogu prilagoditi faktorima životne sredine (uključujući tu i interakciju sa imunskim sistemom domaćina) i to za vreme različitih razvojnih faza (Ding J. i sar., 2017).
Nakon momenta izleganja gastrointestinalni trakt pilića biva sukcesivno kolonizovan prvo bakterijama Enterobacteriaceae u prvim danima života, a potom i bakterijama Firmicutes (aproksimativno od 7. dana starosti) (Ballou A. L. i sar., 2016). Međutim, kolonizacija gastrointestinalnog trakta specifičnim vrstama bakterija, koje pripadaju grupama Enterobacteriaceae ili Firmi-cutes, verovatno je potpuno slobodan i slučajan proces koji pokreće prvi kontakt sa mikroorganizmima koji se nalaze u neposrednom okruženju pilića (životnoj sredini) ili u hrani ili vodi (Kubasova T. i sar., 2019). Postoji potpuna saglasnost u naučnoj zajednici da je rana kolonizacija creva pilića od velike važnosti za kasnije zdravlje i produktivnost živine, jer u suprotnom može izmeniti morfologiju i fiziologiju creva i njegovu osetljivost na zarazne bolesti (Kers J. G. i sar., 2018).
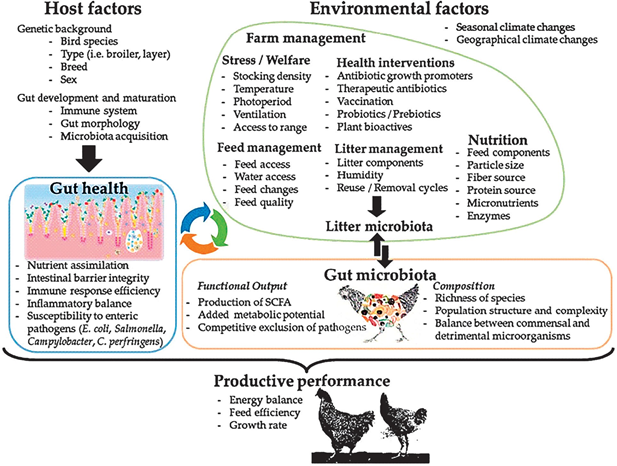
Slika 1. Shema 1. Shema preuzeta od Diaz Carrasco J. M., Casanova, N. A., & Fernández Miyakawa, M. E. (2019): Microbiota, Gut Health and Chicken Productivity: What Is the Connection?. Microorganisms, 7(10), 374
Inokulacija prebioticima, probioticima i grupama mikroorganizama, koji se mogu primeniti direktno na ili unutar jajeta, ocenjuju se kao moguća strategija za favorizovanje rane crevne kolonizacije ptica sa „zdravim“ mikrobiomom i to od momenta izleganja pilića (Rubio L. A., 2019, Baldwin S. i sar., 2018, Simon K. i sar., 2016).
Nakon te početne kolonizacije creva primećuje se sukcesija i izmena mikroorganizama u kojima se bogatstvo vrsta i složenost populacione strukture bakterija u sastavu mikrobiota povećava kako ptice odrastaju sve dok na kraju mikrobiom ne dostigne stanje sazrevanja i velike stabilnosti.
Ovaj proces se normalno odigrava kod komercijalnih brojlerskih pilića u starosti od oko 3 nedelje života (Jurburg S. D. i sar., 2019, Johnson T. J. i sar., 2018). No bez obzira što je ovo opšte pravilo koje važi za komercijalnu brojlersku proizvodnju, moramo uzeti u obzir da vremenski razvoj i obrasci nastanka crevnih mikrobioma mogu u velikoj meri varirati, a sve u zavisnosti od genetske pozadine pilića, kao i drugih faktora upravljanja farmama (Stanley D. i sar., 2014, Ding J. i sar., 2017, Ngunjiri J. M. i sar., 2019, Zou A. i sar., 2018, Pandit R. J. i sar., 2018, Zhao L. i sar., 2013, Keck Z. i sar., 2012).
Na primer, kod kokošaka nosilja su opisane 4 različite faze razvoja mikrobioma slepih creva (cekuma) i to sve tokom prve godine života i koje se sve odlikuju značajnim promenama u njegovom sastavu (Videnska P. i sar., 2014).
Neki naučnici izveštavaju i da su sukcesivne promene mikrobioma creva u korelaciji sa promenama citokinskog profila koji je rezultat ekspresije gen crevnih ćelija domaćina, kao njihovog manifestovanog odgovora na prisustvo različitih grupa bakterija (Oakley B. B. i Kogut M. H., 2016). Porast prisustva bakterija u tipu (phylum) Proteobackteria, koje mogu da uključuju i mnoge potencijalno patogene bakterije, u korelaciji je sa formiranjem proinflamatornog profila citokina, dok je porast bakterija koje pripadaju filumu Firmicutes povezan sa antiinflamatornim statusom organizma. Na taj način je mikrobiom creva uključen u imunološku homeostazu gastrointestinalnog trakta živine, tako da svaka neravnoteža mikrobioma creva može posledično dovesti do imunološkog disbalansa i samim tim i uticaja na zdravlje živine.
Možemo reći da starost živine spada među najvažnije faktore koji utiču na bakterijski sastav intestinalnog mikrobioma živine, gustinu ćelija mikrobioma, kao i njegovu metaboličku funkciju. Sve ove navedene razlike u sastavu intestinalnog mikrobioma živine najčešće se otkrivaju primenom metode poznate kao „sekvenciranje sledeće generacije“ ili NGS (next generation sequencing) koja je opisana od strane velikog broja autora (Shaufi M. A., 2015, Yeoman C. J. i sar., 2012, Stanley D. i sar., 2014, Kers J. G. i sar., 2018).
Ballou i sar. (Ballou A. L. i sar., 2016), ali i noviji podaci Kumara i sar. (Kumar S. i sar., 2018) su dokazali da već prvog dana posle izleganja brojlerski pilići imaju zajednicu mikroorganizama u svom gastrointestinalnom traktu. Otkriveno je da postoji čitav niz sukcesivnih promena u sastavu mikrobioma creva pilića koje nastaju kao posledice zamene i naseljavanja stabilnih bakterijskih „taksona“ (taxa), kako ptice postaju sve starije, odnosno odrastaju (Lu J. i sar., 2003, Crhanova M. i sar., 2011).
Lu i sar. (Lu J. i sar., 2003) su otkrili da gastrointestinalni trakt pilića u uzrastu od 3. dana starosti sadrži sledeće bakterije: L. delbrueckii, C. perfringens i Campylobacter coli, dok su već u uzrastu od 7. do 21. dana starosti češće prisutne sledeće bakterije: L. acidophilus, Enterococcus i Streptococcus. U 28. i 49. danu starosti gastrointestinalni trakt sadrži L. crispatus, ali se ostatak sastava mikrobioma značajno razlikuje u odnosu na sastav u drugim uzrastima (Lu J. i sar., 2003). Dokazano je i još jedno opšte nepisano pravilo (primenom NGS tehnologije sekvenciranja) kada govorimo o sukcesivnim izmenama mikrobioma kod živine, a to je činjenica da je relativno prisustvo bakterija iz roda Clostridium bilo češće kod starijih ptica, dok su bakterije iz roda Lactobacillus tokom starenja živine bile sve manje prisutne u crevnom mikrobiomu živine.
Tang i sar. (Tang H. C. i sar., 2020) su procenjivali efekat na intestinalni mikrobiom brojlera kada su hranjeni hranom u kojoj je dodavana fitaza poreklom od Mitsuokella jalaludinii. Brojleri hranjeni dodatkom ove fitaze su imali bolju konverziju, ali to nije značajno uticalo na sastav bakterija koje ulaze u sastav cekalnog mikrobioma u odnosu na kontrolnu grupu pilića kojima nije dodavana fitaza, te su glavne grupe bakterija i dalje bile prisutne u obe grupe brojlera: Bacteroidetes, Furmicutes i Proteobacteria.
Nikonov I. i sar. (Nikonov I. N. i sar., 2017) su predstavili rezultate molekularno-genetskih analiza promene sastava mikrobioma u crevima nosilja Lohman Brown hibrida tokom njihovog celokupnog odgoja (ontogeneza). Utvrdili su da je preko 70% filotipova bakterija moglo biti svrstano u 3 grupe: Firmicutes, Bacteroidetes i Proteobacteria, a manji broj bakterija je pripadao bakterijama Actinobacteria, Tenericutes i Fusobacteria, uz značajan broj još uvek neidentifikovanih bakterija. Tokom rasta nosilja ptice su ispoljile značajne promene u odnosu na broj prisutnih filotipova u svom crevnom mikrobiomu. U starosti između 20 do 40 nedelja ptice su imale značajan porast bakterija predstavnika klase Clostridia koje imaju ulogu u metabolizmu ugljenih hidrata, potom bakterija koje koriste kiseline iz reda Negativcutes, kao i bakterija sa antagonističkim osobinama (Bifidobacteriales, Bacillus), kao i značajno smanjenje bakterija oportunističkih i patogenih taksona – Enterobacteriaceae, red Pseudomonadales, phylum Tenericutes. Najveća homogenost crevnog mikrobioma je bila u uzrastu od 20 nedelja.
Uticaj sezonskih i klimatskih promena na intestinalni mikrobiom živine
Intenzivni odgoj pilića zahteva rigoroznu kontrolu zoohigijenskih uslova koji vladaju u komercijalnim objektima za odgoj, a sve u cilju optimizacije porasta živine od kojih su glavni temperatura i vlažnost vazduha u živinarnicima (Jones T. A. i sar., 2005) Međutim, čak i regulisanjem uslova sredine unutar živinarnika, spoljni klimatski uslovi, naročito ekstremne vrućine, mogu negativno uticati na zdravlje i produktivnost živine (Farag M. R. i Alagawany M., 2018, Lara L. J. i Rostagno M. H., 2013). U nedavno izvedenoj studiji na farmi brojlera u Argentini je primećeno da postoji velika varijacija u sastavu mikrobioma cekuma u odnosu na godišnja doba i to sa dvostruko većim brojem prisutnih vrsta bakterija u toku leta nego zimi (Diaz Carrasco J. M., 2019). Ovo je u skladu sa nalazima drugih autora koji su primetili sličan sezonski obrazac variranja raznovrsnosti mikrobioma cekuma živine u zavisnosti od porekla uzoraka koji su uzimani od više različitih jata brojlerskih pilića u SAD (Oakley B. B. i sar., 2018). Sa druge strane, postoje mnoga istraživanja koja upućuju na razlike u profilima mikrobioma creva živine, u zavisnosti od geografskog položaja (Siegerstetter S. C. i sar., 2017, Zhou X. i sar., 2016). Verovatno se i ove varijacije intestinalnog mikrobioma mogu delimično pripisati uticaju regionalnih i sezonskih uslova koji okružuju ptice, kao i uslova u samim pticama. Sagledavanje uticaja svih ovih klimatskih uslova, kao i uslova životne sredine, od suštinskog je značaja prilikom osmišljavanja i sprovođenja ispitivanja odnosa između mikrobioma creva i proizvodnih performansi živine.
Uticaj faktora menadžmenta i unutrašnjih uslova na farmama živine
Postoji mnogo faktora povezanih sa internim menadžmentom (upravljanjem) i ustanovljenim načinom odlučivanja u intenzivnoj živinarskoj proizvodnji koji su relevantni za uspostavljanje zdravog crevnog mikrobioma živine. Uticaj nekih faktora na proizvodne osobine brojlerskih pilića je detaljno proučavan (Averós X. i Estevez I., 2018), ali je još uvek malo studija koje analiziraju ove odnose na osnovu sastava i raznolikosti mikrobioma creva. Među najrelevantnijim faktorima uticaja na mikrobiom preko menadžmenta (upravljanja) farmom ističe se primenjeni proizvodni sistem (Ocejo M. i sar., 2019, Shi Z. i sar., 2019), različiti higijenski i biosigurnosni programi, protokoli i kriterijumi koji se koriste da se definišu vreme i pristup hrani, obrada hrane i programi hranjenja (Jha R. i sar., 2019, Mohammadi Ghasem Abadi M. H. i sar., 2019, Metzler-Zebeli B.U. i sar., 2019), protokoli i kriterijumi koji se koriste da definišu program vakcinacije, sprovođenje lečenja, sprovođenje godišnje rotacije antibiotskih promotora rasta (ako se koriste), faktora povezanih sa stresom i dobrobiti životinja, kao što je gustina naseljenosti živine (Guardia S. i sar., 2011, Wu Y. i sar., 2018), svetlosni program (Wang J. i sar., 2018, Hieke A. i sar., 2019), ventilacija i koncentracija amonijaka u vazduhu (An Y. i sar., 2019, Tao Z. i sar., 2019) i toplotni stres (Shi D. i sar., 2019, He J. i sar., 2019). Jasno je da odluke menadžmenta utiču i definišu i sam mikrobiom u životnoj sredini koja okružuje pticu, kao i mikrobiom creva ptice, ali je potrebno uraditi više ispitivanja u komercijalnim uslovima proizvodnje živine da bi se utvrdile ključke tačke koje doprinose održavanju zdravog mikrobioma creva i maksimiziranja proizvodnih rezultata živine.
Kao potvrdu ove prethodne teze iznećemo rezultate nekoliko istraživanja uticaja promene hrane na mikrobiom živine. U radu Zdunczyk i sar. (Zduńczyk Z. i sar., 2016) su samo delimičnom zamenom mlevene pšenice (brašnast oblik) celim zrnom pšenice u hrani za ćurke izazvali pozitivne promene u njihovom mikrobiomu creva. U drugoj studiji Zdunczyk i sar. (Zduńczyk Z., 2013) su uključivanjem 22,5% pšenice u zrnu u hrani za ćurke posledično uvećava procenat prisustva Bacteriapan> i Bifidobacterium spp., a u isto vreme umanjuje broj Salmonella spp., ali i uvećava sadržaj korisnih jedinjenja: buterne kiseline i ukupnih kratkolančanih masnih kiselina u sadržaju cekuma. Jankowski i sar. (Jankowski J. i sar., 2013) su postepenim uvećanjem sadržaja pšenice u zrnu u hrani ćuraka doveli do značajnog umanjenja broja bakterija i to Escherichia coli, Clostridiaceae i Clostridium perfrigens.
Sistem živinarske proizvodnje koji se primenjuje u proizvodnji jaja (kavezni ili slobodni, odnosno podni sistem) ima veliki uticaj na formiranje i sastav mikrobioma. Shi i sar. (Shi S. i sar., 2019) su, zbog činjenice da sistemi gajenja nosilja imaju važnu ulogu u dobrobiti nosilja, njenom zdravlju, kao i sastavu mikrobioma slepih creva, odlučili da ispitaju efekte različitih sistema gajenja nosilja na sastav mikrobioma slepih creva i to kod nosilja u 120. danu starosti (Lohman hibrida) koje su bile gajene u kavezima i koje su gajene na podnom sistemu. Ispitivanje je vršeno sekvenciranjem bakterijskog fragmenta ribozoma (16S rRNK) i to primenom NGS. Tri najzastupljenije grupe bakterija ustanovljene su kod oba sistema gajenja: Bacterioidetes (više od 48%), Firmicutes (više od 37%) i Proteobacteria (više od 6%), dok su bakterije grupe Defferibacteres bile otkrivenje u podnom sistemu gajenja (više od 2,4%), a skoro da nisu detektovane u kaveznom sistemu gajenja (manje od 0,01%). Tri najzastupljenija roda su bila: Bacteroides, Rikenellaceae i Faecalibacterium. Dokazano je i relativno često prisustvo Parabacteroides i Prevotellaceae. Neklasifikovani predstavnici Proteobacteria, a neklasifikovane bakterije iz Spirachaetaceae su bile češće kod podnog sistema gajenja, dok je prisustvo Faecalibacterium, Ruminococcaceae i Helicobacter bilo veće u kaveznom sistemu gajenja. Sekvenciranjem je generalno detektovano veće prisustvo funkcionalnih gena važnih u produkciji energije, transportu i metabolizmu ugljenih hidrata, kao i aminokiselinskom transportu i metabolizmu i to kod nosilja gajenih u podnom sistemu. Time je dodatno potvrđena velika razlika u sastavu crevnog mikrobioma živine u zavisnosti od sistema gajenja.
Međusobna zavisnost i uticaj između mikrobioma creva živine i mikrobioma prostirke
Dolaskom jednodnevnih pilića (bez prethodnog kontakta sa odraslim pticama) na farmu, oni bivaju izloženi mikrobiomu životne sredine od kojih je prostirka najvažnija te stoga predstavlja važan faktor u oblikovanju mikrobioma pilića koji će oni nositi tokom čitavog života. To dokazuje i činjenica da je preko 50 rodova bakterija zajedničko za prostirku, feces i leševe ptica. Važno je napomenuti da je primećeno da se bakterijski sastav (mikrobiom) fecesa mnogo brže, lakše i češće menja, nego što je to slučaj sa mikrobiomom cekuma koji je mnogo stabilniji po sastavu. Ne treba ispustiti iz vida da taksonomske promene ne moraju obavezno značiti i promene u metaboličkoj funkciji ili morfološkom razvoju creva i na tom odnosu i principima treba tek raditi u budućim istraživanjima.

Prostirka na kojoj se uzgajaju pilići se obično sastoji od usitnjenog drveta i drugih biljnih materijala (npr. slame), ali i od hrane, vode i izlučevina pilića koji se pomešaju i kompostiraju sa biljnim materijalom u prostirci. Materijali koji se koriste za prostirku mogu bitno izmeniti morfologiju i fiziologiju creva, kao i sam sastav mikrobioma creva (Wang S. i sar., 2018). Kroz ciklus odrastanja, ptice kontinuirano kljucajući unose partikule prostirke i tim putem dobijaju važan deo mikroorganizama koji čine mikrobiom creva. Zauzvrat, prostirka akumulira fekalne materije i stvara mikrobiom sa svojim sopstvenim sastavom i raznolikošću (Pan D. i Yu Z., 2014). U jednom radu je praćeno u toku jedne kalendarske godine, 6 posebnih uzastopnih ciklusa proizvodnje brojlera pri čemu je otkrivena bliska povezanost između mikrobioma cekuma i mikrobioma prostirke, sa istim sezonskim obrascem varijacije diverziteta u oba mikrobioma (Diaz Carrasco J. M., 2019). Iako je populaciona struktura veoma različita, određene grupe bakterija su zajedničke i ispoljavaju isti model (oblik) varijacija u obe sredine: i u živini i u prostirci. Drugi autori su opisali da je mikrobiom u prostirci u korelaciji sa odgovarajućim mikrobiomom creva i to kod dve ispitivane vrste: kokošaka i ćuraka (Mancabelli L. i sar., 2016, Danzeisen J. L. i sar., 2015). Pored toga, neki autori su dokazali da su sezonske promene mikrobioma prostirke u korelaciji i sa sezonskim promenama u produktivnosti jata, koja je redovno bolja zimi a lošija leti. Ovo je povezano sa uvećanjem raznolikosti bakterijskih vrsta u mikrobiomu cekuma i to po istom sezonskom modelu (Diaz Carrasco J. M., 2019). Ta međusobna veza oslikava stalnu razmenu mikroorganizama koja normalno postoji između mikrobioma koji postoji u životnoj sredini unutar farme i mikrobioma creva živine i ističe važnost uloge prostirke kao rezervoara mikrobne raznolikosti.
Ponovna upotreba stare prostirke (korišćene prethodno) tokom useljavanja svih uzastopnih jata živine se obično primenjuje radi smanjenja proizvodnih troškova živinarske proizvodnje u mnogim zemljama. Postoje objavljeni rezultati koji dokazuju da ovakva praksa može izmeniti mikrobiom u samoj prostirci gde se povećava prisustvo (prevalenca) halotolerantnih/alkalofilnih bakterija, ali se menja i mikrobiom creva živine tako što se uvećava nivo Faecalibacterium prausnitzii, vrste bakterije (komensala) koji proizvodi buternu kiselinu, u cekumu mladih pilića (Wang L. i sar., 2016). Neki drugi autori su dokazali da je broj crevnih bakterija veći u već korišćenoj prostirci, kao i u onoj prostirci koja ima veći sadržaj vlage, sugerišući da to može značiti i veći rizik po zdravlje živine, pre svega zbog mogućeg prenošenja patogena sa jednog jata na drugo preko korišćene prostirke (Wang L. i sar., 2016, Oakley B. B. i sar., 2013). Iako je ovaj rizik teorijski razuman, potrebno je uraditi više studija da bi razumeli kako balans između komensala, probiotika i patogenih bakterija u prostirci može uticati na zdravlje, odnosno stanje mikrobioma creva živine.
Uticaj antibiotika na sastav intestinalnog mikrobioma i imuniteta
Modifikacija mikrobioma creva u ranom životu pilića upotrebom antibiotika per oralnim putem je povezana sa kasnijom pojavom disfunkcije imuniteta živine, uključujući i mogući razvoj autoimunih bolesti (Arrieta M.-C. i sar., 2014). Promene u inflamatornom odgovoru creva, isto kao i u strukturi i raznolikosti crevne zajednice mikroba, takođe se javljaju kada su antibiotici bili uvedeni preko hrane živine (Khadem A. i sar., 2014, Soler L. i sar., 2016, Pourabedin M. i sar., 2015, Neumann A.P. i Suen G., 2015, Bosi P. i sar., 2011, Kaukas A. i sar., 1988, Engberg R. M. i sar., 2000, Dumonceaux T. J. i sar., 2006, Pedroso A. A. i sar., 2006, Wise M. G. i Siragusa G. R., 2007, Zhou H. i sar., 2007, Lin J. i sar., 2013). Takođe je dokazano da antibiotski tretmani povećavaju prevalencu i osetljivost domaćina na druge crevne patogene (Arrieta M. C. i sar., 2014, Kumar S. i sar., 2018). Antibiotici su u niskim koncentracijama najčešće korišćeni u živinarskoj industriji širom sveta (pa su zato i ispitivani) kao stimulatori rasta. Korišćen je metabolički pristup za karakterizaciju i identifikaciju biohemijskih komponenti prisutnih u crevima brojlerskih pilića hranjenih standardnom hranom sa dodatkom antibiotika, kao promotorima rasta, virginiamicina ili bacitracin metilen disalicilata i utvrđeno je da dodavanje antibiotika ima značajne efekte na nivou velikog broja hemijskih metabolita, posebno aminokiselina, masnih kiselina, nukleozida i jedinjenja srodnih nikotinamidu (Gadde U. D. i sar., 2018). Podržavajući ideju postojanja antiinflamatornog efekta antibiotika koji su dodati kao promotori rasta (Calder P. C., 2017), zapažen je uticaj na proizvodnju peptidnih medijatora upale (adhezioni molekuli, citokini, itd.) (Calder P. C., 2017). Ptice hranjene dodatkom bacitracin metilen disalicilata su imale raznolikost mikroorganizama i bogatstvo bakterijskih vrsta slično kontrolnim životinjama, ali je antibiotik uticao na sastav bakterijskih zajednica u cekumima i ileumu (Kumar S. i sar., 2018, Díaz Carrasco J. M. i sar., 2018). Velike bakterijske grupe (filumi) nisu pretrpeli uticaj bacitracina u hrani, ali su promene u prisutnim bakterijskim populacijama bile primetne na nižem taksonomskom nivou, na primer na nivou roda (Kumar S. i sar., 2018, Díaz Carrasco J. M. i sar., 2018). Međutim, ove promene u bakterijskim zajednicama su bile u korelaciji i sa ekspresijom gena pojedinih citokina (IL-10, IL-4, IFN-γ), posebno u različitim fazama rasta pilića. Produkcija citokina može biti modulirana i komensalskim bakterijama u gastrointestinalnom traktu (Corthay A., 2006).
Pojačana ekspresija gena za IL-4 i IL-10 u ranoj fazi rasta, koja se smanjivala u kasnijim fazama, primećena je kod pilića (Kumar S. i sar., 2018). Ove promene se mogu pripisati promenama u zajednici mikroorganizama koje su nastale kao posledica starosti, ali verovatno i zbog dodavanja antibiotika ili infekcije patogenima kao što su Campylobacter ili Salmonella (Kumar S. i sar., 2018). Ekspresija citokina, kao odgovor na infekciju sa Campylobacter jejuni, kod pilića zaraženih u kasnijem uzrastu je veća za IL-6, IL-17A i IL-17F (Connerton P. L. i sar., 2018, Reid W. D. K. i sar., 2016). Vreme izlaganja bakteriji C. jejuni menja profil ekspresije citokina kroz sam ciklus rasta ptice i zauzvrat, ovaj imunološki odgovor može dovesti do promena u čitavom sastavu mikrobioma creva (Connerton P. L. i sar., 2018). Slično tome, opisana je korelacija između profila citokina pilića i njihove rezistencije na infekciju sa Salmonella typhimurium (Connerton P. L. i sar., 2018). Međutim, promene drugih članova mikrobioma, kao što je Escherichia coli, takođe su u korelaciji sa većom osetljivošću na kolonizaciju vrstama Salmonella (Stecher B. i sar., 2010) i izolatima Lactobacillusa koji su bili u mogućnosti da kontrolišu Salmonella infekcije kod pilića (Yang X. i sar., 2014). Ovi primeri ilustruju složenost interakcija koje posto je u mikrobiomu creva živine i koliko je teško definisati specifične efekte koje izazivaju određeni mikroorganizmi. Ne samo patogeni, već i različiti komensali koji su članovi mikrobioma creva, u mogućnosti su da izmene imunski odgovor živine. Withanage i sar. su izvestili da se ekspresija IL-6 uvećava u cekalnim tonzilama, ileumu i slezini prvog i trećeg dan posle infekcije kada su jednodnevni pilići bili inficirani sa Salmonella typhimurium (Withanage G. S. K. i sar., 2005).
Mnogi gram-negativni patogeni, kao što su E. coli, Shigella, i Salmonella su Proteobacteriae sa prepoznatim proinflamatornim mehanizmima. Mada nijedan specifičan rod bakterija nije bio u značajnoj korelaciji sa ekspresijom citokina, najbrojniji rodovi u okviru grupe (phylum) Proteobacteria su bile klasifikovane kao Escherichia/ Shigella (Oakley B. B. i sar., 2016). Među bakterijama Firmicutes modulacija ekspresije citokina varira u zavisnosti od vrste bakterije koja se analizira. Nekoliko rodova, uključujući rod Faecalibacterium, bilo je u obrnutoj korelaciji sa ekspresijom proinflamatornih citokina (IL-1β, IL-18, IL-6) i u pozitivnoj korelaciji sa antiinflamatornom ekspresijom citokina TGF-β4, dok su ostale bakterije grupe Firmicutes imale pozitivnu korelaciju sa ekspresijom proinflamatornih citokina (Oakley B. B., 2016). Postoji relativno obilje bakterija grupe (phylum) Bacteroidetes, koja obično predstavlja drugu najbrojniju grupu u mikrobiomu cekuma, posle grupe Firmicutes, gde dominira rod Bacteroides, koji ima različitu korelaciju sa antiinflamatornim citokinima u skladu sa starošću ptice (Oakley B. B., 2016).

Korelacija između sastava intestinalnog mikrobioma i proizvodnih performansi živine
Veza između raznolikosti bakterijskih vrsta u mikrobiomu creva živine i efikasnosti ishrane živine nije tako jasna. Kod goveda je detektovana manja raznolikost mikrobioma buraga. Brojni autori su postavili hipotezu da je ovaj odnos povezan sa specijalizacijom mikrobioma goveda u produkciji izlaznih metabolita koji su mnogo relevantniji za ukupan metabolizam energije domaćina i to uglavnom preko kratkolančanih isparljivih masnih kiselina koje mogu biti korišćene kao izvor energije i ugljenika za rast životinje (Shabat S. K. i sar., 2016). U skladu sa ovim konceptom, neki autori su izvestili o nižoj raznovrsnosti mikroorganizama u crevima one živine koja ima veću efikasnost ishrane, ali ne i kada su analizirani uzorci fecesa živine (Siegerstetter S. C. i sar., 2017, Bae Y. i sar., 2017). Nekoliko drugih studija je dokazalo da je bakterijska raznolikost u okviru intestinalnog trakta veća kod ptica sa nižom konverzijom ili sa većom efikasnošću ishrane (Stanley D. i sar., 2013, Yan W. i sar., 2017, Torok V. A. i sar., 2011, Stanley D. i sar., 2012, Singh K. M. i sar., 2012). Na rezultate izučavanih mikrobioma živine su uticale karakteristike ptica kao što su genetika, pol, starost, rasa i zdravstveni status, ali isto tako i spoljašnji uslovi na farmi koji uključuju ishranu, aditive hrane, životnu sredinu i sistem upravljanja. U Tabeli 2. su prikazani mikrobiološki taksoni koji su povezani sa visokom i niskom produktivnošću živine u različitim delovima gastrointestinalnog trakta živine.
Tabela 2. Mikrobiološki taksoni koji su povezani sa visokom i niskom produktivnošću kod živine.
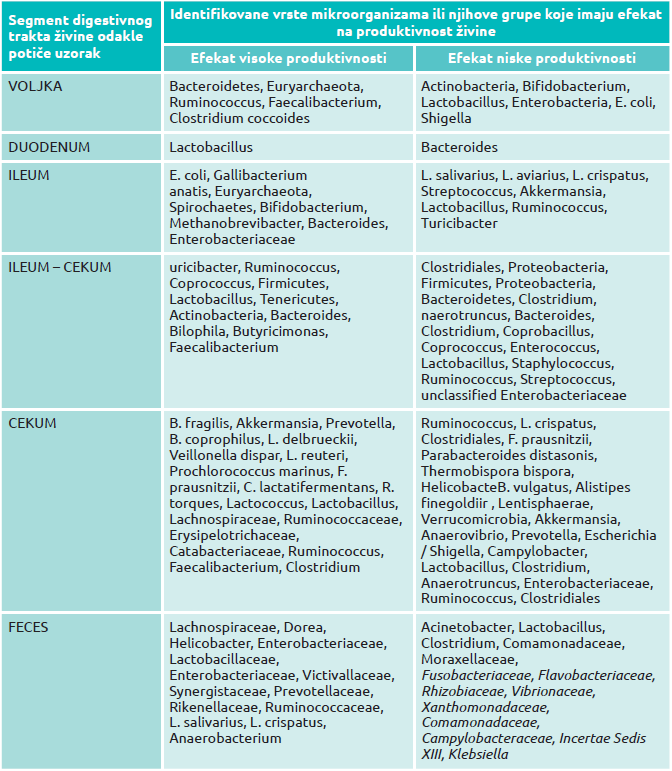
U uzorcima iz jejunuma studije nisu detektovale razlike u sastavu mikrobioma živine sa visokim i niskim performansama produktivnosti (Stanley D. i sar., 2012, Torok V. A. i sar., 2008). U ileumu je detekcija različitih bakterijskih taksona bila povezana sa produktivnošću pilića. Suprotno očekivanjima, dve odvojene studije su povezale prisustvo enterobakterija sa visokom produktivnošću i prisustvo laktobacila sa niskom produktivnošću (Tabela 2.). Iako je ovaj rod bio povezivan sa zdravstvenim statusom ptica i njihovom visokom produktivnošću, niska raznolikost može dovesti do porasta određenih bakterija povezanih sa nastankom nekih bolesti (Ocejo M. i sar., 2019). Cekumi su delovi creva sa najvećom bakterijskom raznolikošću kod živine i tu je više razlika, u sastavu mikrobioma, bilo detektovano u odnosu na efikasnost iskorišćavanja hrane kod pilića. Takvi potencijali su bili dodeljeni bakterijskim vrstama kao što su Lactobacillus salivarius, Lactobacillus aviarius, Lactobacillus crispatus, Clostridium lactatifermentans, članovi familije Ruminococcaceae, Bacteroides vulgatus, Akkermansia i Faecalibacterium (Yan W. i sar., 2017, Torok V. A. i sar., 2011, Han G. G. i sar., 2016).
Prisustvo Escherichia i Shigella je u negativnoj korelaciji sa rastom i svarljivošću masti kod brojlerskih pilića (Rubio L. A. i sar., 2015). Takođe je kolonizacija bakterijom Campylobactera kod brojlerskih pilića dovedena u vezu sa smanjenjem ekonomske isplativosti tova živine u smislu uvećanja utroška hrane i smanjenja konverzije (Awad W. A. i sar., 2015, Chaloner G. i sar., 2014). U jednom drugom radu, ponovljena ispitivanja u odvojenim jatima brojlera su bila izvedena da uporede sastave mikrobioma cekuma kod živine sa visokim i niskim proizvodnim rezultatima (Stanley D. i sar., 2016). Autori su otkrili razlike između bakterijskih grupa koje su povezane sa konverzijom hrane. Štaviše, svaki rezultat produktivnosti je bio u različitoj korelaciji sa specifičnim prisutnim filotipovima bakterija, čak i pod kontrolisanim uslovima. U svim slučajevima, Lactobacilli su bili u korelaciji sa visokom, dok je rod Faecalibacterium bio u korelaciji sa niskom konverzijom hrane. U novijim studijama, restriktivni pristup hranjenju je bio sproveden sa ciljem da se razjasni utucaj unošenja hrane na mikrobiom ileuma i mikrobiom cekuma, kao i fiziološke i funkcionalne karakteristike kod brojlerskih pilića sa različitim unosom hrane kao merom efikasnosti proizvodnje (Metzler-Zebeli B. U. i sar., 2019, Siegerstetter S. C. i sar., 2018). Ovi autori su opisali da su predominantne familije kao što su Turicibacteraceae, Ruminococcaceae i Entero-bacteriaceae bile u većoj meri pod uticajem restriktivnog hranjenja u oba pomenuta dela creva (ileumu i cekumu), bez obzira na rezultat u konverziji hrane. Ovo ispitivanje je uključivalo žrtvovanje dela ptica, pa se praćenje promena crevnog mikrobioma u toku nastavka ogleda, vrši kod pojedinačno drugih ptica. To očekivano uvodi veću varijabilnost u rezultate ispitivanja usled individualnih razlika među njihovim mikrobiomima. Uprkos prednostima analize kloakalnih briseva, kao metode uzorkovanja, intestinalni mikrobiom dobijen na ovaj način ne odražava uvek različitost koja se opaža u različitim segmentima intestinuma živine (Johnson T. J. i sar., 2018, Videvall E. i sar., 2018). Stanley i sar. su dokazali da upotreba fekalnog brisa kao metode uzorkovanja može biti korisna za kvalitativno praćenje mikrobioma cekuma, ali podsećaju da je potrebno proučiti veliki broj uzoraka zbog toga što pražnjenje različitih delova gastrointestinalnog trakta uvodi značajnu varijabilnost u podatke (Stanley D. i sar., 2015). Drugi autori su uporedili sastav uzoraka fecesa u grupama sa različitom efikasnošću i detektovali slično obilje Lactobacillusa i Bacteroides u odnosu na nivo ispoljenih proizvodnih performansi (Singh K. M. i sar., 2012). Acinetobacter, Anaerosporobacter i Arcobacter su bili obilno prisutni u niskoefikasnoj grupi, dok su Enterobacteriaceae i Faecalibacterium bili prevalentni u efikasnijoj grupi pilića. Međutim, postoje dokazi da relativno obilje nekih bakterija u fecesu nije u korelaciji sa sastavom dobijenim iz tankog ili debelog creva (Yan W. i sar., 2017, Siegerstetter S. C. i sar., 2017).
Wen i sar. (Wen C. i sar., 2019) su identifikovali 2 mikrobiološka taksona Methanobrevibacter i Mucispirillum schaedleri čije je prisustvo bilo u značajnoj korelaciji sa obimom taloženja masti. Pilići sa manjim procentom bakterija Methanobrevibacter su imali znatno niži sadržaj nataložene abdominalne masti od onih kod kojih je zabeleženo veće prisustvo bakterije Methanobrevibacter (35,51 g : 55,59 g), dok se telesna masa pilića nije razlikovala. Pilići sa većim procentom Mucispirillum schaedleri su imali niži stepen akumulacije abdominalne masnoće (39,88 g : 55,06 g), ali i nižu telesnu masu (2,23 kg : 2,41 kg) od onih kod kojih je bilo registrovano manje prisustvo ove bakterijske vrste. Ovi nalazi mogu pomoći razvijanju strategije pravaca izmene mikrobioma živine kako bi se kontrolisalo taloženje masti.
Koliko može oblik hrane uticati na promenu mikrobioma creva, a posledično i na proizvodne performanse, svedoči i rad Yun i sar. (Yun J. i sar., 2019) koji su ispitivali efekat primene fermentisane hrane na sastav cekalnog mikrobioma gusaka, kao i njegovu povezanost sa proizvodnim rezultatima. Četiri grupe gusaka su hranjene sa različitim procentom udela fermentirane hrane u obrocima i to: 0,0%, 2,5%, 5,0% i 7,5%. Rezultati su dokazali da je grupa sa najvećim udelom fermentisane hrane (7,5%) imala veću telesnu masu kao i dnevni prirast. Takođe, u toj grupi gusaka, u odnosu na kontrolnu grupu (0,0%), bio je veći udeo bakterija iz grupe Bacteroidetes, dok je prisustvo bakterija iz grupe Firmicutes bilo znatno manje. Kod iste grupe gusaka (hranjenih fermentiranom hranom), na nivou roda, bilo je registrovano veće prisustvo bakterija Bacteroides, dok je prisustvo Desulfovibrio, Phascolarctobacterium, Lachnospiraceae, Ruminiclostridium i Oscillospira bilo manje. Jasno je da rezultati ukazuju na to da fermentirana hrana ima važan efekat na mikrofloru slepih creva gusaka, a time i na porast domaćina, kao i na zdravlje creva.

Mikrobiom creva živine i produktivnost živine su blisko povezani i ta povezanost je dosta dobro proučena. Međutim, nalazi su ponekad kontradiktorni ili neubedljivi i teško je identifikovati specifičnu bakterijsku populaciju koja bi mogla reproducibilno poboljšati neki pokazatelj produktivnosti i modulirati mikrobiom živine na željeni način ako znamo da su uzročno-posledični odnosi još uvek nejasni. Potrebna su dodatna ispitivanja da razviju inovativne alate i tehnologije koje bi doprinele poboljšanju neinvazivnog monitoringa mikrobioma creva.
Jedan od najvažnijih zaključaka prilikom realizacije projekta ispitivanja mikrobioma ljudi je da je jasno dokazano da postoji „konzervacija metaboličkih funkcija“ uprkos velikoj taksonomskoj varijabilnosti kod pojedinaca (Turnbaugh P. J. i sar., 2007). Identičan zaključak se može izvesti i analizom postojećih javno dostupnih podataka o živini. Praktično, to znači da analizom velike količine podataka i kod živine, kao i kod ljudi, slične metaboličke funkcije mogu obavljati i mikrobiološke zajednice (mikrobiomi) koji se po filogenetskom sastavu sastoje od veoma različitih vrsta mikroorganizama. Sve to ukazuje na moguće mehanizme lateralnog prenošenja funkcionalnih gena odgovornih za proizvodnju određenih metaboličkih produkata i to između više veoma različitih taksona bakterija, verovatno zbog toga što su stalno pod određenim pritiskom, kako organizma domaćina, tako i međusobno.
Perspektiva upotrebe prebiotika i probiotika kao načina za kontrolu, „krojenje“ i razvoj mikrobioma u željenom pravcu
Prebiotici
Veliki broj studija je dokazao da performanse rasta, iskoristivost hraniva, kao i zdravstveni status creva kod brojlerskih pilića mogu biti poboljšani dodavanjem prebiotika, nesvarljivih ugljenih hidrata koji selektivno stimulišu umnožavanje korisnih mikroorganizama. Na primer dodavanje 0,4% fruktooligosaharida u koncentrat za brojlere značajno utiče na povećanje telesne mase, iskorišćavanje hrane, aktivnosti proteaza i amilaze, visinu crevnih resica, kao i porast brojnosti vrsta Bifidobacterium i Lactobacillus. Slično dodavanje mananoligosaharida (MOS) u hranu za brojlere je imalo za posledicu povoljan efekat kroz poboljšanje procesa obezbeđenja dovoljno energije. Svarljivost proteina, vlakana i ugljenih hidrata je veća, kao i njihova upotrebljivost (Oakley B. B. i sar., 2014).
Upotreba prebiotika kao potencijalnog modulatora mikrobioma ispoljila je pozitivne efekte na neke vrste bakterija u kolonu (Gaggia F. i sar., 2010). Tako fruktooligosaharidi (FOS) i galaktooligosaharidi (GOS) uvećavaju populaciju Bifidobacteriuma i Lactobacillusa (Jung S. J. i sar., 2008, Xu Z. R. i sar., 2003). In vitro izvršeno ispitivanje smeše, koja se sastojala od kaše fecesa inkubiranog sa dodatkom oligofruktoze i inulina poreklom iz humanog kolona, dokazalo je ukupno povećanje udela populacije bifidobakterija, dok su potencijalni patogeni kao što su Escherichia coli i Clostridium spp. imali značajno niži nivo udela u ovakvom mikrobiomu u odnosu na kontrolni (samo kaša fecesa) (Nywang X. i Gibson G. R., 1993). Većina sojeva bifidobakterija (kao što su B. fiagilk, B. thetaiotaomicron, B. vulgatus, B. dktasonk i B. ovatus) izuzev B. bifidum, može koristiti FOS kao promoter rasta i procesa fermentacije (Hidaka H. i Hirayama M., 1991). Pomenute bakterije luče enzim ß-fruktozidazu koja može razgraditi i fermentisati FOS. Mikroorganizmi kao što su E. coli i C. perfringens nemaju sposobnost da koriste FOS kao izvor ugljenih hidrata. Pacovi koji su bili hranjeni hranom sa dodatkom FOS-a su imali privremeni porast bakterija koje produkuju mlečnu kiselinu i dugoročno povećanje buterne kiseline u cekumu (Le Blay G. i sar., 1999).
Ishrana koja uključuje dodatak FOS smanjuje populaciju C. perfringens i E. coli i uvećava diverzitet Lactobacillusa u gastrointestinalnom traktu brojlera (Kim H. J. i sar., 2011).
Drugi tip prebiotika, manooligosaharidi (MOS), imaju različite mehanizme delovanja. Oni mogu delovati na neki od sledećih načina: 1. vezati se za potencijalno patogene gram-bakterije (E. coli i Salmonella spp.) koje poseduju fimbrije tipa 1 (manoza senzitivan lektin), sprečavajući tako vezivanje patogena za zid creva, 2. imaju efekat imunomodulatora baziranog na antigenim osobinama komponenti glukana i manana, 3. menjaju morfologiju intestinuma i 4. povećavaju ekspresiju mucina smanjujući stepen brzine zanavljanja enterocita (Yang Y. i sar., 2009). Efekat prebiotika na niže partije gastrointestinalnog trakta uključuje sledeće: 1. služe kao hrana i izvor procesa fermentacije za mikrobiom cekuma i kolona, 2. produkciju krajnjih proizvoda fermentacije (na primer kratkolančane masne kiseline), 3. stimulisanje saharolitičke fermentacije, 4. zakišeljavanje sadržaja velikih creva, 5. hiperplaziju epitela cekuma i kolona, 6. stimulaciju sekrecije hormonskih peptida kolona i 7. ubrzanje prolaska sadržaja kroz cekume (Gaggia F. i sar., 2010).
Probiotici
Probiotici su najefikasniji za vreme početnog razvoja mikrobiota ili posle bilo kakvih promena hrane, stresa ili davanja antibiotika, kada je potrebno brzo i efikasno ponovo uspostaviti normalnu mikrofloru creva.

Brojne studije su dokazale da dodavanje probiotika koji sadrži Lactobacillus kulture u hranu za brojlere povećava njihov prirast, odnosno povećava telesnu masu, povećava iskoristivost hrane i smanjuje mortalitet pilića. Još krajem XX veka, je izveden eksperiment sa dodavanjem mešavine 12 sojeva Lactobacillusa pilićima u tovu. To je dovelo do smanjenja masnih naslaga u abdomenu, snižavanja nivoa holesterola u krvi, snižavanja nivoa triglicerida i boljih proizvodnih performansi (Oakley B. B. i sar., 2014).
Kod miševa i ljudi, bakterije Firmicutes su pokazale pozitivan efekat na iskoristivost energije iz hrane, uz obavezno dobar odnos Firmicutes : Bacteroides, koji se pokazao kao vitalan za optimalnu fiziologiju i dobru ishranu, odnosno optimalno dejstvo probiotika.
Uvećanje broja Firmicutes bakterija u fecesu uvećava resorpciju hranljivih sastojaka, dok je povećanje broja bakterija Bacteroidetes povezano sa smanjenjem resorpcije hranljivih materija. Kao probiotski sojevi koji utiču na proizvodne performanse brojlerskih pilića najvažnije su sledeće bakterije: Lactobacillus salivarius, L. aviarius, L. crispatus, Faecalibacterium prausnitzii, E. coli, Gallibacterium anatis, Clostridium lactatifermentans, Ruminococcus torques, Bacteroides vulgatus i Alistipes finegoldii (Oakley B. B. i sar., 2014).
Treba obavezno imati u vidu da prisustvo Lactobacillus spp. u nižim delovima tankih creva živine utiče na smanjenje performansi kod pilića, jasno stavljajući do znanja koliko je važna i lokalizacija gde će se bakterija umnožiti (Oakley B. B. i sar., 2014).

Umesto zaključka
Poslednjih godina je napravljen značajan napredak u razumevanju taksonomskog sastava mikrobioma digestivnog trakta živine i njegove uloge u zdravom i normalnom funkcionisanju creva. U narednom periodu je važno da se nastave započeta istraživanja, kako bi se uvećalo naše poznavanje i razumevanje uloge mikrobioma creva u ishrani, zdravlju, bolesti i produktivnosti živine. Napredak u poznavanju ove oblasti nauke će nam pomoći da bolje razumemo kako da upravljamo mikrobiomom creva na osnovu životne sredine, ishrane i fizioloških promena kod ptica i kako da dalje unapredimo naše sposobnosti da modifikujemo mikrobiom i njegove metaboličke uloge. Time možemo da doprinesemo novim načinima i mogućnostima za poboljšanje zdravstvenog stanja živine.
Postoji mnogo velikih izazova u razumevanju gastrointestinalnog mikrobioma živine, ali optimizacija taksonomskog sastava i biohemijskih funkcija gastrointestinalnog mikrobioma živine predstavljaju realan cilj i izazov za postgenomsku eru. Ovi podaci demonstriraju važnost mikrobioma u očuvanju intestinalne homeostaze, kao i raspoložive alate za njegovo moduliranje kojima se utiče na produktivnost pilića i verovatno je da će praćenje sastava mikrobioma creva na farmama u budućnosti biti rutinski izvođeno.
Ovaj članak daje pregled sadašnjih saznanja o funkciji gastrointestinalnog mikrobioma živine, kao i faktorima koji utiču na njegovu raznovrsnost. U njemu se objašnjava najnoviji pristup koji se koristi u istraživanju intestinalnog mikrobioma živine.
Bolje razumevanje funkcije i mikrobiologije creva živine obezbediće nam nove pogodnosti za poboljšanje zdravlja živine i njenih proizvodnih rezultata i što je najvažnije, osigurati bezbedniju i kvalitetniju hranu za ljude. Možemo sa sigurnošću očekivati da će unapređenje u strategijama koje omogućavaju poboljšanje zdravlja creva živine i predstavljati svojevrsni menadžment mikrobiomom creva. To može da bude alternativa upotrebi antibiotika, uz unapređenje primene prebiotika i probiotika, poboljšanje kvaliteta upravljanja polimikrobnim zaraznim bolestima živine i samim tim, boljom kontrolom mnogih humanih patogena, što će dodatno unaprediti javno zdravlje.
*** Literatura je dostupna kod autora e-mail: sekler@vsikv.com